

Никелевые аноды для гальваники
ГОСТ 2132-2015 Аноды никелевые. Технические условия
В гальваническом производстве достаточно часто применяют никель как защитно-декоративное покрытие на стали, меди и алюминии. Никелирование всегда ведут с растворимыми анодами - пластинами из практически чистого никеля, который растворяется в электролите под током и затем электрокристаллизуется на катоде.
Никель для гальваники производится в виде анодов различных марок: НПА-1 (99,7 % Ni), НПА-2 (99 % Ni), НПАН (непассивирующиеся) (99,4% Ni). В качестве добавок, препятствующих пассивации анодов (депассиваторов) вводят 0,002-0,01 % S (в виде сульфидов) и 0,03-0,3 % О (в виде оксидов). После прокатки НПАН закаливается, в результате чего структура металла измельчается.
|
Марка
|
Ni+Co, %
|
Максимальное содержание примесей, % |
||||||||
|
Fe
|
Si
|
Mn
|
Mg
|
Cu
|
S
|
C
|
O
|
Сумма
|
||
|
НПАН
|
>99,4
|
0,10
|
0,03
|
0,05
|
-
|
0,01-0,1
|
0,002-0,010
|
-
|
0,03-0,30
|
0,60
|
|
НПА1
|
>99,7
|
0,10
|
0,03
|
0,10
|
0,10
|
0,10
|
0,005
|
0,02
|
-
|
0,30
|
|
НПА2
|
>99,0
|
0,25
|
0,15
|
0,15
|
0,10
|
0,15
|
0,005
|
0,10
|
-
|
1,00
|
Аноды изготавливаются в виде прямоугольных или овальных полос, которые также могут нарубаться для засыпки в анодные корзины.
Предпочтительнее, безусловно, аноды, содержащие в себе большую концентрацию никеля и меньшую концентрацию примесей, которые могут негативно отразиться на работе ванны.
Никелевые аноды под током растворяются неравномерно и образуют шлам. Главной причиной шламообразования является разнородность кристаллической решетки анодов на уровне зёрен металла (кристаллитов), заключающаяся в большом различии их размеров. Логично, что в первую очередь растворяются мелкие зёрна, а более крупные не успевают раствориться и выкрашиваются, переходя в анодный шлам.
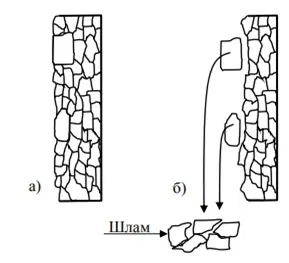
Наличие примесей в никелевых анодах также приводит к неравномерному их растворению. Особенно опасны магниевые, углеродные и серные включения.
Магний приводит к образованию сквозных дыр в анодах.
Углерод создает локальные короткозамкнутые гальванические элементы, что также способствует неравномерному растворению никелевых анодов.
Сера в анодах приводит к образованию сульфидов никеля, которые растворяется легче, чем чистый никель. Сульфиды распределены в аноде по границам зерен, все это существенно повышает шламообразоование.
Учитывая, что классические электролиты никелирования активно перемешиваются, шлам легко распределяется по объему ванны и включается в растущий осадок, в основном на внешних горизонтальных участках деталей. В дальнейшем встроенные в покрытие частички разрастаются, что еще больше увеличивает шероховатость. При попытке зашлифовать неоднородности может произойти выламывание кристалликов, на месте которых останутся ямки, иногда доходящие до металла - основы. Полировка же таких дефектов бесполезна — полировальные круги будут эффективно истираться, оставляя на обрабатываемой поверхности кусочки волокон и полировальной пасты.
Наибольшему шламообразованию подвержены крупнозернистые и неоднородные литые аноды. Мелкокристалличные горячекатанные в этом смысле предпочтительнее.
Никелевые аноды, кроме шламления при работе склонны к пассивации. При этом они переходят в нерастворимое состояние и на них начинает выделяться газ - кислород и, если в состав ванны входят хлориды - хлор.
Явление пассивации анодов приводит к нарушению состава электролита (никель будет израбатываться, а кислотность - расти). Пассивное состояние анодов поддерживается малорастворимыми солями никеля, образующимися на их поверхности при превышении допустимой анодной плотности тока. С момента начала пассивации анод становится все более электроположительным и начинается реакция:
Ni - 3ē → Ni3+
Ионы трехвалентного никеля гидролизуются:
Ni3+ + 3OH- → Ni(OH)3
Ni(OH)3 → Ni2O3 + H2O
Образующийся диэлектрик Ni2O3 способствует еще более глубокой пассивации.
При пассивировании анодов в растворе очень быстро растет содержание ионов водорода и уменьшается концентрация никеля. Из-за проблемы с пассивацией возникает необходимость добавления в электролит активирующих добавок - ионов Cl-. Однако их добавление делает электролит агрессивным как в отношении оборудования, так и в отношении покрываемых изделий. Растворение сорвавшихся с подвесок деталей в электролите с хлоридами идет активнее, что приводит к загрязнению электролита железом, медью, цинком и т.д.
Литые аноды легче растворяются, чем катаные. Часто применяют комбинированное завешивание литых и катаных анодов. Иногда рекомендуют в аноды вводить примеси других металлов, например железа. Однако, широко пользоваться этим на практике неудобно, так как катодное осаждение никеля чувствительно к присутствию в электролите примесей.
На рисунке ниже приведена типичная анодная поляризационная кривая в растворе сульфата никеля без хлоридов, полученная в потенциостатическом режиме. На ней: Eoc - потенциал разомкнутой цепи; Epp - основной или критический потенциал пассивации; Ep - потенциал пассивации; ioc - коррозионная плотность тока; ipp - основная плотность тока пассивации; ip - плотность тока в пассивной области. AB является активной областью, BC - область перехода от активного к пассивному состоянию, и С - начало области пассивации
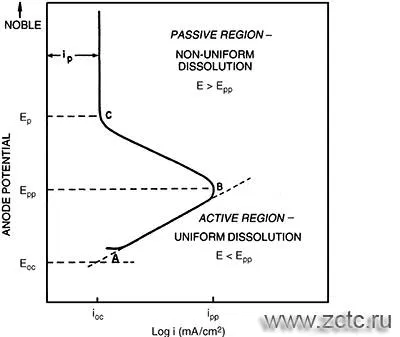
При введении 14 г/л хлоридов анодная поляризационная кривая меняет ход (рН=4, температура 55° С). Ниже приведены кривые, полученные в потенциостаттическом и потенциодинамическом режиме.
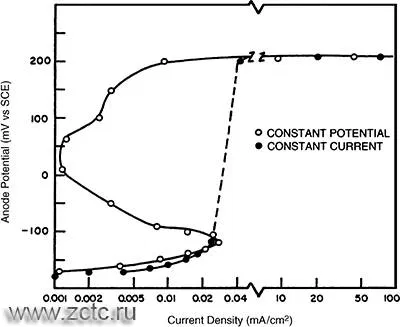
Разбирая процессы, протекающие на аноде при их пассивировании, и активирующую роль хлор-иона, Ферстер и Кригер считали, что препятствия к переходу никеля в раствор могут встречаться при наличии разряда на аноде хлор-ионов до газообразного хлора. Препятствия, нарушающие непосредственное анодное растворение никеля могут быть преодолены, если никель будет быстро реагировать с очень низкими концентрациями хлора и заметно деполяризовать разряд хлор-ионов:
NiCl2 → Ni2+ + Cl- (1)
Но активное состояние на аноде будет продолжаться до тех пор, пока скорость процесса не отстанет от скорости процесса разряда хлор-ионов.
При недостаточном выделении на аноде хлора роль последнего могут взять на себя сульфат-ионы, как это бывает при электролизе разбавленной серной кислоты с никелевыми анодами:
Ni + SO42- → Ni2+ + SO42- (2)
Последняя реакция протекает значительно медленнее, чем реакция (1), и по мере накопления сульфат-ионов у анода начинается разложение его по уравнению:
SO42- + H3O → 2H+ + SO42- + O (3)
Благодаря выделению кислорода наступает явление пассивности и в дальнейшем будет протекать следующий процесс:
Ni2+ - e → Ni3+ (4)
Но трехвалентные ионы никеля неустойчивы, и при недостатке кислоты на аноде идет реакция:
Ni3+ + 3H2O → Ni(OH)3 + 3H+ (5)
Образующаяся при этом темно-коричневая перекись никеля покрывает частично анодную поверхность, делая ее неэлектропроводной, отчего рабочая анодная поверхность уменьшается, а плотность тока растет, и поэтому легко протекает реакция (3) и (4). В то же время, образующиеся согласно процессу (4) ионы трехвалентного никеля могут реагировать с имеющимися в растворе хлор-ионами:
Ni3+ + Cl- → Ni2+ + Cl (6)
отчего равновесие (5) смещается влево; пленка, состоящая из Ni(OH)3 сперва разрыхляется, а затем растворяется. Вследствие увеличения рабочей поверхности плотность тока понижается и наступает активное состояние. Последнее состояние будет поддерживаться до тех пор, пока уменьшение концентрации хлор-ионов на определенных участках анодной поверхности благодаря неравномерной плотности тока снова не приведет к пассивному состоянию. Такие чередующиеся явления характеризуют переходящую пассивность. В тех случаях, когда концентрация хлор-ионов настолько мала, что она даже приблизительно не соответствует применяемой плотности тока, на аноде будет иметь место преимущественный разряд сульфат-ионов с выделением газообразного кислорода, и незначительное растворение никеля т.е. наступает явление полной пассивности.
Читайте также статьи
Заказать гальваническое никелирование (Н.б)
Сделать заказ никелирования с сертификатом качества на заводе
Техпроцесс никелирования
Описание процесса осаждения гальванического никеля. Свойства покрытия.
Система менеджмента качества по ИСО 9001
Политика в области качества ООО

Хотите стать нашим клиентом?
Просто оставьте Вашу заявку, заполнив форму справа и мы свяжемся с Вами в ближайшее время. Спасибо!

Отправляя заявку, Вы даете согласие на обработку Ваших персональных данных. Ваши данные под защитой.



