

Технология и составы ванн для электрохимического полирования нержавеющей стали.
Влияние факторов процесса на результаты электрохимического полирования нержавеющей стали.
Важными факторами, влияющими на внешний вид электрохимполированной поверхности, являются тип, форма и плотность тока, состав электролита, перемешивание и температура ванны, продолжительность процесса:
- С повышением температуры увеличивается скорость растворения металла, усиливается блеск деталей и становится возможным снизить плотность тока.
- Повышение плотности тока увеличивает скорость сглаживания и позволяет сократить продолжительность полирования. Чрезмерно высокая плотность тока может вызвать интенсивное выделение кислорода, что может привести к появлению поверхностных дефектов.
- Состав электролита, плотность тока и скорость перемешивания являются взаимодополняющими. Если вязкость раствора увеличивается (в результате добавления молочной, щавелевой кислоты или глицерина), содержание адсорбированного количество частиц на поверхности электрохимически отполированного металла может увеличиваться, что в конечном итоге приводит к снижению шероховатости.
- Электропроводность ванны зависит от концентрации ее компонентов и температуры.
- Повышенная температура существенно влияет на электропроводность раствора и снижает напряжение при электролизе.
Наилучшие результаты процесса электрополировки достигаются после выполнения трех основных этапов:
- Подготовка поверхности (мойка, промывка, маринование, промывка)
- Электрохимическая полировка (полировка, выявление элементов, промывка);
- Окончательная обработка (промывка в серной кислоте VI, промывка, горячая промывка, сушка, проверка качества
Промывка элементов из нержавеющей стали разбавленной серной кислотой дополнительно помогает очистить поверхность элемента от загрязнений, которые могут появиться в результате электрохимической полировки. После каждого этапа обработанные элементы промываются деминерализованной водой.
Для создания тонкого вязкого слоя из продуктов анодного растворения на поверхности анода в электролите требуется поддерживать низкую концентрацию ионов железа и хрома. С этой целью после подготовки ванны ее “обрабатывают” для получения определенной, низкой концентрации этих ионов в растворе.
Во время электрополировки концентрация ионов металлов в электролите увеличивается и изменяется его вязкость. Содержание растворенного железа в ванне влияет на удельный вес, кислотность и вязкость раствора, а также на выход по току. На практике известно, что при содержании железа в электролите 3% по массе (приблизительно 70 г/л) процесс электрохимической полировки прекращается. В таком случае ванну следует регенерировать или заменить.
Ресурс ванн для электрохимической полировки обычно определяется величиной тока прошедшего тока через единицу объема ванны с момента ее приготовления. Например, электролиты для электрохимической полировки углеродистой стали “живут” от 100 до 180 А*ч/л.
Уход за ванной обычно заключается в удалении 30-50% объема раствора после отработки примерно 80 А*ч/л и последующем дополнении его свежим раствором. Ванны для полировки хромовой и никелевой стали более долговечны. Их поддержание заключается в регулярном добавлении придающих блеск добавок (например, триэтаноламина) в количестве, вдвое меньшем, чем указано в рецептуре.
Состав ванн электрохимической полировки нержавеющих сталей.
Основными компонентами растворов, используемых для электрохимической полировки нержавеющей стали, являются серная и ортофосфорная кислота. Серная кислота обеспечивает надлежащую высокую электропроводность раствора, в то время как фосфорная кислота отвечает за свойства прианодного слоя.
Во время электрополировки нержавеющей стали компоненты стали растворяются:
Fe → Fe3+ + 3e- (8)
Cr → Cr3+ + 3e- (9)
Ni → Ni2+ + 2e- (10)
2H2O → O2 + 4H+ + 4e- (11)
На катоде выделяется водород:
2H3О+ + 2e- → 2H2O + H2 (12)
Элементы, изготовленные из хромоникелевой стали, могут подвергаться электрохимической полировке в ваннах, содержащих серную кислоту, ортофосфорную кислоту, триэтаноламин, этиленгликоль, щавелевую кислоту и ацетанилид. Нержавеющая сталь также может быть подвергнута электрохимической полировке в растворе, состоящем из серной кислоты и лимонной кислоты, а также из серной, фосфорной и молочной кислоты. Некоторые другие составы включают: 2-амино-2-метил-1-пропанол, этаноламин, диэтаноламин, глицерин и фосфат натрия. До недавнего времени также использовались соединения хромовой кислоты (VI).
Эббот в своих исследованиях предложил ванну, состоящую из ионных жидкостей этиленгликоля и хлорида холина, вместо ванн, приготовленных из водных растворов кислот. Эта смесь CHCl:EG может быть потенциальной альтернативой электролитам на основе серной/фосфорной кислот для электрохимической полировки нержавеющей стали. Механизм электрополировки в водных растворах кислот отличается от такового в смеси CHCl:EG. Удаление оксида происходит медленнее и в большей степени зависит от потенциала анода, чем в водных растворах. Когда оксид будет удален с поверхности, атомы металла окисляются, и процесс обработки начинает контролироваться массопереносом.
При электролитической полировке нержавеющих сталей в промышленных масштабах используются только водные растворы, которые представляют собой концентрированные растворы фосфорной и серной кислот, иногда с добавками.
Элиаз, Ниссан и Соджитра представили процесс электрохимической полировки имплантатов, изготовленных из стали 316L, в растворах, которые менее вредны для окружающей среды, то есть в ваннах, состоящих из серной кислоты 96% (50% об.) и фосфорной кислоты 85% (50% об.). Хайдопулос и Чжао провели исследование ванны, состоящей из 99% глицерина (47-50% об.), фосфорной кислоты 85% (35-42% об.) и дистиллированная вода. Эти ванны использовались для электрополировки стентов, изготовленных из стали 316L. Перед электрохимической полировкой образцы подвергали протравливанию в ваннах, состоящих из азотной и фтористоводородной кислот. Параметры процесса для первой ванны были следующими: температура 75°C, плотность тока 0,44 А/см2, продолжительность 3 минуты. Вторая ванна работала при температуре 90-95° C, при этом плотность тока составляла 1,2 А/см2, а время - 1-10 мин. Ванны для образцов и параметры процесса электрохимического полирования нержавеющей стали представлены в таблице 1.
| Материал | Ванна | Режим работы (параметры) | ||
| Сталь AISI 304, 316 | j (A/дм2) | t (мин) | T (°C) | |
| Серная кислота (VI) (35 мас.%), ортофосфорная кислота (V) (51 мас.%), триэтаноламин 99%. (3 мас.%),H2O (11 мас.%) | 20 | 12 | 55 | |
| Серная кислота (VI) 96% (40% об.), ортофосфорная кислота (V) 85% (60% об.), добавки: этиленгликоль 99% — 200 г/дм3, щавелевая кислота — 200 г дм3, ацетанилид — 200 г/дм3. | 35-50 | 1-50 | 60 | |
| Серная кислота (VI) 96% (50% об.), ортофосфорная кислота (V) 85%, (50% об.) | 15 | 1-3 | 40-75 | |
| Ортофосфорная кислота (V) 85% (35% об.), глицерин 99% (50% об.), дистиллированная вода (15% об.) | 75 | 1-10 | 60-95 | |
| Базовый раствор: ортофосфорная кислота 85%: серная кислота (VI) 97% при соотношении от 2:1 до 3:2; (75% об.), глицерин 99% (25% об.) | 50 | 1-10 | 30-90 | |
Шероховатость поверхности стентов после травления в плавиковой и азотной кислоте составила Ra = 126,07 ± 37,13 нм. Кислотное травление проводилось для удаления шлака и присоединившихся оксидов металлов после других видов обработки поверхности (например, лазерной микрообработки) перед электрохимической полировкой. Электрополировка стентов в первом растворе привела к шероховатости поверхности Ra = 14,77 нм при выбранных рабочих параметрах, в то время как шероховатость после электрохимической полировки во второй ванне составила Ra = 13,13 нм. Потеря веса в первой ванне после травления составила 7,43%, в то время как после процесса электрохимической полировки - 17,99%. Во втором случае потеря массы после травления составила 7,7% и 16,7% после электрохимической полировки.
Электрохимическая полировка и другие методы обработки поверхности
Основываясь на литературных данных, было определено, что выбор подходящего метода обработки поверхности зависит от размера и внутренней структуры элементов. Во многих случаях электрохимическая полировка предпочтительна для использования объектов сложной формы, поскольку механическая полировка очень сложна.
Лукас Лебер в своих исследованиях представил способ обработки поверхности элементов, изготовленных из стали 316L размерами 10×10×10 мм. Чтобы уменьшить шероховатость, обрабатываемые элементы изготавливались с помощью технологии SLM (селективное лазерное плавление). Эти образцы были подвергнуты следующей механической обработке: струйной очистке, шлифованию, механической полировке, а также электрохимической полировке и электроплазматической полировке (таблица 2).
| Метод | Величина абразива | Шероховатость, мкм |
| SLM | 15,03 | |
| Шлифовка | Р 80 | 2,22 |
| Р 240 | 1,15 | |
| Р 300 | 0,52 | |
| Р 500 | 0,43 | |
| Пескоструйная очистка со стеклом | 50-150 мм | 8,85 |
| Электрохимполировка после SLM | 15,03 | |
| Шлифовка и электрохимическая полировка | Р 80 | 9,28 |
| Р 240 | 1,46 | |
| Р 500 | 0,64 | |
| Механическая полировка и электрохимическая полировка | - | 0,21 |
| Механическая полировка и электроплазменная очистка | - | 0,12 |
Положительные эффекты были получены после сочетания механической полировки с электрополировкой: параметр шероховатости Ra снизился с 15,03 мкм до 0,21 мкм и после механической полировки в сочетании с электроплазменной полировкой, после которой шероховатость составила 0,12 мкм.
Таблица 3, составленная на основе обзора литературы. Ток- I – ток, А, U – напряжение, В, j – плотность тока А/см2 или А/дм2, q – количество пропущенного электричества, А*ч/см2, T – температура, оС, t – время, с, мин или ч.
| Параметры процесса полировки | Состав ванны | Типы анализов/Материал | Результаты |
| Т = 40, 50, 58, 67° С, U = 2–4 В, I = 0,04 А, j = 0,15 А/см2, t 10 мин, S = 0,27 см2, q 24,7 мАч/см2. | H2SO4 96%, H3PO4 85% (50% по объему). | Шероховатость поверхности/316LVM. | Средняя шероховатость: АСМ: SS: Ra = 18,4 4,5 нм, после ЭП: Ra = 2,1±0,8 нм. Профилометр: SS: Ra = 183,1±80,6 нм, после ЭП: Ra = 76,2± 67,9 нм. |
| U = 10–12 В, I = 1,2 А, T = 90–95°C, t = 1 мин, S — поверхность одного стента. | H3PO4 85% (42 мас.%), глицерин (47 мас.%), H2O (11 мас.%). | Шероховатость поверхности/316L. стенты: длина 15 мм, диаметр 1,6 мм, толщина стенки 95 мкм. | Средняя шероховатость: (а) центральная часть образца: SS: Ra = 120,52±26,65 нм, травление: Ra = 126,07±37,13 нм, релаксация: Ra = 142,71±26,20 нм, после ЭП: Ra = 13,13±1,56 нм, (б) лазер площадь резания: SS: Ra = 491,26±52,46 нм, травление: Ra = 268,67±27,7 нм, релаксация: Ra = 302,90±23,33 нм, после ЭП: Ra = 15,01±1,79нм |
| U = 9,5 В, I = 0,44 А, T = 75°C, t = 3 мин, S — поверхность одного стента. | H2SO4 96%, H3PO4 85% (50% по объему). | Шероховатость поверхности, коррозионная стойкость/316LVM, стенты: длина 16 мм, диаметр 1720 мм, толщина стенки 110–115 мкм. Коррозионные испытания проводились в фосфатно-солевом буферном растворе (PBS) при pH 7,4 и постоянной температуре 37±1 C. Потенциал холостого хода измеряли в течение 1000 с относительно насыщенного каломельного электрода (SCE). | Результат обработки: снижение шероховатости на 78,10%: SS: Ra = 250 нм, после EP: Ra = 14,77 нм, SS: Rq = 97,56 нм, после EP: Rq = 4,895 нм, SS: Rp = 208,7 нм после EP: Rp = 32,49 нм, SS: Rv = 130 нм, после ЭП: Rv = 8,921 нм. Коррозионный потенциал: - после травления: Ecor = 326 мВ, - после лазерной резки: Ecor = 259 мВ, - после ЭП: Ecor = 173 мВ. |
| I = 6,8 А, j≤40 А/дм2, T = 55±1°C, t = 4, 6 мин, S = 20 см2, q≤40 мАч/см2. |
1 – H3PO4 (51 мас.%), H2SO4 (35 мас.%), H2O (14 мас.%), 2 – H3PO4 (51 мас.%), H2SO4 (35 мас.%), глицерин (3 мас.% ), Н2О (11 мас.%). 3 – H3PO4 (51 мас.%), H2SO4 (35 мас.%), триэтаноламин (3 мас.%), H2O (11 мас.%). Другие органические добавки: триэтиламин, этаноламин, диэтаноламин, бутилдигликоль |
Шероховатость поверхности, коррозионная стойкость, блеск/образцы из стали 304, размеры: 90х25х1,5 мм. | Ванна 1: протравленная: Ra = 0,35–0,38 м, после ЭП: (q = 0,02 Ач/см2) Ra = 0,12 м, после ЭП: (q = 0,03 Ач/см2) Ra = 0,10 м, после ЭП: (q = 0,04 Ач/см2) Ra = 0,12 м. Блеск: (t = 6 мин, j = 30 А/дм2, q = 0,03 Ач/см2) = 890±10 GU. Ванна 2: протравленная: Ra = 0,36–0,40 м, после ЭП: (q = 0,02 Ач/см2) Ra = 0,14 м, после ЭП: (q = 0,03 Ач/см2) Ra = 0,10 м, после ЭП: (q = 0,04 Ач/см2) Ra = 0,09 м. Блеск: (t = 6 мин, j = 30 А/дм2, q = 0,03 Ач/см2) = 680±10 GU. Ванна 3: протравленная: Ra = 0,36–0,38 м, после ЭП: (q = 0,02 Ач/см2) Ra = 0,095 м, после ЭП: (q = 0,03 Ач/см2) Ra = 0,09 м, после ЭП: (q = 0,04 Ач/см2) Ra = 0,079 м. Блеск: (t = 6 мин, j = 30 А/дм2, q = 0,03 Ач/см2) = 900±20 GU. Рекомендуемые параметры обработки: ванна 3, j = 30 А/дм2, T = 55 C, t = 6 мин. |
| U = 2,5; 4; 10 В, Т = 65–70°С, t = 3 мин, S = 3,33 см2. | H3PO4 85 % (60 % по объему), H2SO4 95–97 % (20 % по объему), глицерин 99,5 % (10 % по объему), H2O (10 % по объему). | Шероховатость поверхности, коррозия, химический состав поверхности, адгезия клеток крови/316L, диаметр 12,7 мм, толщина стенки 2 мм. Коррозионные испытания проводились в 0,16 М растворе NaCl. | SS: Ra = 188±9 нм, после ЭП: (U = 2,5 В) Ra = 107 6 нм, после ЭП: (U = 4 В) Ra = 77±4 нм, после ЭП: (U = 10 В) Ra = 97±11 нм. Потенциал коррозии: SS: OCP = 0,34 В, после EP: (U = 2,5 В) OCP = 0,29 В, после EP: (U = 4 В) OCP = 0,18 В, Снижение адгезии: после EP: (U = 2,5 В) ) на 71 %, после ВП: (U = 4 В) на 89 %, после ВП: (U = 10 В) на 93 %. |
| U = 10 В, T = 60°C, (ЭПО – потенциал выделения кислорода), T = 25 °C (ЭПБО – плато выделения кислорода), t = 5 мин. | 1—H3PO4 85%, H2SO4 93%-7:3 об. (ЭПО), 2 – 100 мл CH3OH, 300 мл H2SO4 93% (ЭПВО). | Шероховатость поверхности, коррозионная стойкость, химический состав поверхности, адгезия клеток/316L Коррозионные испытания проводились в фосфатно-солевом буферном растворе (PBS) при pH 37 °C при постоянной температуре. В качестве электрода сравнения использовали каломельный электрод (КЭЭ), а в качестве противоэлектрода использовали графитовый стержень. | SS: Ra = 33,51 ± 5,54 нм, после ЭПО: Ra = 11,50 ± 1,61 нм, после EPBO: Ra = 6,07 ± 0,73 нм, SS: Rq = 48,28 ± 8,65 нм, после EPO: Rq = 14,79 ± 1,90 нм, после EPBO : Rq = 7,91 ±0,73 нм. Плотность тока коррозии: SS: jcorr = 56,1 мА/м2, после EPO: jcorr = 23,7 мA/м2, после EPBO: jcorr = 12,9 мA/м2, коррозионный потенциал: SS: Ecor = 410 мВ, после EPO: Ecor = . 353 мВ, после EPBO: Ecor = α288 В, Скорость линейной коррозии: SS: Vp = 0,0475 мм/год, после EPO: Vp = 0,0182 мм/год, после EPBO: Vp = 0,0123 мм/год, Сопротивление поляризации: SS: Rs = 93,40ΩВтсм2, после ЭПО: Rs = 104,2 ВтΩсм2, после ЭПВО: Rs = 100,8 ВтΩсм2, Химический состав поверхностного оксидного слоя (XPS): SS: Fe2p = 13,89 мас.%, после ЭПО: Fe2p = 10,51 мас.% , после ЭПВО: Fe2p = 11,5 мас.%, SS: Cr2p = 1,86 мас.%, после ЭПО: Cr2p = 7,55%, после ЭПВО: Cr2p = 8,55 мас.%, после ЭПВ: Cr2p3 = 5,65 мас.%, после ЭПВО : Cr2p3 = 1,23 мас.%, SS: O = 43,92 мас.%, после ЭПО: O = 36,51 мас.%, после ЭПВО: O = 38,75 мас.%. |
| U = 5 В, I = 0,6 А, j = 25 А/дм2, T = 50 °C, t = 20 мин, S = 2,4 см2, q ≤ 83 мАч/см2. | H3PO4 (60% по объему), H2SO4 (40% по объему). | Шероховатость поверхности, коррозионная стойкость, химический состав поверхности, адгезия ячеек/316L, 10 х 10 х 1 мм. Коррозионные испытания проводились в растворе Рингера при постоянной температуре 37 °С. Хлорсеребряный электрод (Ag/AgCl) и платиновый противоэлектрод использовали в качестве электрода сравнения и рабочего электрода. | SS: АСМ Sa = 161,34 ± 57,15 нм, после ЭП: Sa = 5,05 ± 0,28 нм, после ЭП + хим. обработка: Sa = 0,96 ± 0,29%, SS: Srms = 206,58 ±70,06 нм, после ЭП: Srms = 8,43 ± 0,40 нм, после ЭП + хим. обработки: Srms = 1,71 ± 0,78%, Плотность тока коррозии: SS: jkor = 0,921 µА/см2, после ЭП: jkor = 0,61 µА/см2, после ЭП + хим. обработки: jkor = 0,0066 µА/см2 , Коррозионный потенциал: SS: Eкор = -343 мВ, после ЭП: Eкор = -292 мВ, после ЭП + хим. обработки: Eкор = α16 мВ, XPS: SS: S = 80,2 ат.%, после ЭП: S = 40,8 ат.%, после ЭП + хим. обработка: S = 37 ат.%, SS: O = 19,8,2 ат.%, после ЭП: O = 49 ат.%, после ЭП + хим. обработка: O = 44,2 ат.% , Fe: после ЭП: Fe = 3,4 ат.%, после ЭП + хим. обработка: Fe = 3,2 ат.%, Cr: после ЭП: Cr = 4,2 ат.%, после ЭП + хим. обработка: Cr = 6,0 ат.% , P: после ЭП: P= 2,7 ат. %, после ЭП + химическая обработка: P = 9,2 ат. %, Жизнеспособность клеток: ок. 80 % (образцы, подвергнутые электрохимической и химической обработке). |
| Т = 20–90 °С, I = 1,5 А, j = 0,75 А/см2, t = 1–6 мин, S = 2 см2 (погружная поверхность) q ≤75 мАч/см2. | глицерин 99% (50% по объему), H3PO4 85% (35% по объему), H2O (15% по объему). | Шероховатость поверхности, химический состав поверхности/316, размеры образцов: 15 х 10 х 1,5 мм. | АСМ: SS: Ra = 2,2 ± 0,15 нм, грунт: Ra = 2,3 ± 0,2 нм, механическая полировка: Ra = 0,04 ± 0,01 нм, после ЭП: Ra = 0,07 ± 0,02 нм. Химический состав – увеличение ат.% Cr с 5,7 % до после ЭП 10 % (для Т = 20 °С) и до 11,5 % (для Т > 20 °С). Рекомендуемые параметры: t = 3 мин, T = 90 °C. |
| Для ванн 1 и 2 ЭП: I = 4 А, j = 20 А/дм2, Т = 55 °С, t = 1–20 мин, Для ванны 3 ЭП: Т = 90 °С, t = 120 мин, S = 20 см2 , q _ 66,7 мАч/см2. | 1: - H2SO4 96% (35% по объему), H3PO4 85% (60,5% по объему), триэтаноламин 99% (4,5% по объему). 2: - H2SO4 96% (40% об/об), H3PO4 85% 60% об/об, гликоль 99% 200 г/дм3, щавелевая кислота 200 г/дм3, ацетанилид 200 г/дм3. 3: - глицерин 99% (50% об/об), H3PO4 85% (35% об/об), H2O (15% об/об). | Шероховатость поверхности, химический состав ванны/316L, размеры образца: 80 х 20 х 2 мм. | SS: Ra = 0,17–0,20 мкм, Ra для ванны 1 после ЭП: Ra = 0,063–0,065 мкм, Ra для ванны 2 после ЭП: Ra = 0,091–0,096 мкм, Ra для ванны 3 после ЭП (при 90 °С): Ra = 0,070 мкм.Рекомендуемые параметры для ванн 1 и 2: t = 15–20 мин, T = 55 °С. Рекомендуемые параметры для ванны 3: T = 90 °C. |
| j = 20 А/дм2, T = 55 °C, t = 12 мин. | H3PO4 (51 мас.%), H2SO4 (35 мас.%), триэтаноламин (3 мас.%), H2O (мас.% 11). | Шероховатость поверхности/загрязнение ванны/304. | SS: Ra = 0,17–0,25 мкм, протравленные: Ra = 0,37–0,43 мкм, после ЭП в промваннах I и II: Ra = 0,14–0,20 мкм (при содержании железа 35–55 г Fe/дм3), после ЭП в промышленная ванна III: Ra = 0,17–0,28 мкм (при содержании железа: 67–75 г Fe/дм3), после ЭП в лабораторной ванне с пониженным содержанием железа (3–6 г Fe/дм3): Ra < 0,11 мкм. |
| j = 0,5–3,0 А/см2, T = 50–95 °C, t = 3, 6, 9 мин. | H2SO4: H3PO4 (об.): 5:5, 4:6, 3:7, H2O, глицерин. | Шероховатость поверхности, коррозионная стойкость/316L Коррозионные испытания проводились в растворе FeCl3 (заготовка заглублялась на 2 см). Контейнер герметизировали и поддерживали температуру на уровне 50°С в течение 72 часов. | Rmax = 0,8 мкм, Ra = 0,08 мкм (для рекомендуемых параметров), Рекомендуемые параметры: j = 1 А/см2, T = 85 °C, t = 3–5 мин, Состав ванны: H2SO4; H3PO4 – об. 4:6, добавление 10% H2O. |
| j = 0,8 А/см2, T = 40 °C, t = 420 с. | H3PO4 (64 мас.%), H2SO4 (13 мас.%), H2O (23 мас.%). | Шероховатость поверхности, коррозионная стойкость/316L. Для испытаний на коррозию в качестве электрода сравнения использовали насыщенный каломельный электрод (НКЭ), а в качестве противоэлектрода использовали платиновую фольгу. Опыты проводили в физиологическом растворе, представленном 0,9 % раствором NaCl. | SS: Ra = 0,256 мкм, после ЭП: Ra = 0,078 мкм, SS: Rq = 0,363 мкм, после ЭП: Rq = 0,096 мкм, SS: Rz = 2,290 мкм, после ЭП: Rz = 0,474 мкм. |
| j = 10, 29, 48, 67 А/дм2, T = 35, 45, 55, 65 °C, t = 3, 14, 25, 36 мин. | 1 – H2SO4 15%, H3PO4 63%, H2O 22%, 2 – H2SO4 35%, H3PO4 45%, H2O 17%, CrO3 3%, 3 – H2SO4 35%, H3PO4 45%, H2O 20%. | Шероховатость поверхности, химический состав ванны/316л. | Максимальные диапазоны Ra после EP: 80–90% для: Рекомендуемые параметры: j = 48 А/дм2, T = 35 °C, t = 25 мин, DRa лучший в ванне 3, худший в ванне 1. Добавление CrO3 в ванну 2 сделало не влияет на результат электрохимической полировки. |
| j = 30–50 А/дм2, T = 55 °C, t = 5–20 мин, S = 4 см2, q = 167 мАч/см2. | H3PO4 (51 мас.%), H2SO4 (35 мас.%), триэтаноламин (3 мас.%), H2O (11 мас.%). | Коррозионная стойкость, химический состав поверхности/304 При коррозионных испытаниях испытуемым электродом служила сталь 304, эталонным насыщенным каломельным электродом (НКЭ) и противоэлектродом был платиновый электрод. | SS: Epit = 0,30 В, травленый: Epit = 0,38 В, после ЭП (для t = 6 мин, j = 30 А/дм2): Epit = 0,57 В, после ЭП (для t = 5 мин, 20 мин, j = 50 А/дм2): Epit (в течение 5 мин) = 0,60 В, Epit (в течение 20 мин) = 0,49 В, ат.% SFe (FeO, Fe2O3, Fe3O4, FeOOH): ТС: ат.% SFe = 6,1%, протравленный: ат.% SFe = 11,9%, после ЭП: ат.% SFe = 14,5%, ат.% SCr (CrO2, Cr2O3, CrO3, Cr(OH)3): SS: ат.% SCr = 18,0%, протравленный : ат.% SCr = 17,9%, после ЭП: ат.% SCr = 28,6%. |
| U = 25 В, T = 30 °C, t = 20 с. | HClO4 70% (20% по объему), CH3COOH 98% (80% по объему). | Коррозионная стойкость, химический состав поверхности/316L, размеры образца: 10 х 10 х 1 Коррозионные испытания проводились при 30 хC в растворе состава вода, т.е. 1000 мг/л B в виде H3BO3 и 2 мг/л Li как LiOH. Электродом сравнения служил насыщенный каломельный электрод (НКЭ), противоэлектродом служила платиновая пластина. | XPS-анализ: после ЭП: ат.% Cr (гидроксид) ≈35%, ат.% Cr (оксид) ≈ 7%, механическая обработка: после ХПС (полировка коллоидным силикатом) ат.% Cr (оксид) ≈ 30%, после ЭП: ат.% Fe (гидроксид) ≈11%, ат.% Fe (оксид) ≈25%, механическая обработка: после УПС: ат.% Fe (оксид) ≈ 28%, коррозия: после ЭП: Rs = 8736 Вт_см2 , после КФС: Rs = 8840 ВтΩсм2, после ЭП: С1 = 78,2 Ф/см2, после КФС С1 = 42,5 Ф/см2, после ЭП: R1 = 0,41 ВтΩсм2, после КФС R1 = 0,97 ВтΩсм2, после ЭП: С2 = 63,8 Ф/см2 /см2, после СУЗ С2 = 35,9 μF/см2, после ЭП: R2 = 3,04 ВтΩсм2, после СУЗ R2 = 5,69 ВтΩсм2. |
| - | - | Коррозионная стойкость/316L, стенты: Коррозионные испытания проводились в растворе тирода при постоянной температуре 37 °C. Каломельный электрод (КЭЭ) в качестве электрода сравнения и платиновая пластина в качестве вспомогательного электрода. | Коррозионная стойкость: После механической обработки: Eкор = 0,533 В, после ЭП: Eкор = 0,324 В, После механической обработки: Vкор = 0,04 мм/год, после ЭП: Vкор = 0,119 мм/год. |
| U = 3 В, j = 1,25–25,5 А/дм2, t = 5–25 мин. | H3PO4 (55 мас.%), H2SO4 (14 мас.%), H2O (31 мас.%). | Блеск, коррозионная стойкость, химический состав, адгезия/304. | SS: Глянец G = 400, после ЭП: G = 1700–2500. Химический состав: мас.% Увеличение содержания Cr после ЭП: с 18,83% до 19,33%. |
| j = 15,5; 31,0; 46,5 А/дм2, Т = 333, 343, 353 К, t = 5–12 мин. | 1 – H3PO4 (500 мл/л), H2SO4 (360 мл/л), моноэтаноламин 20 (мл/л), 2 – H3PO4 (500 мл/л), H2SO4 (360 мл/л), диэтаноламин 20 мл/л, 3 – H3PO4 (500 мл/л), H2SO4 (360 мл/л), триэтаноламин 20 мл/л. | Блеск, состав ванны/304, размеры образца: 25 х 25 х 1 мм. | Ванна 1: (9 мин, 31 А/дм2 при 333, 353 К) – коэффициент отражения = 98 %, ванна 2: (46,5 А/дм2) – максимальный коэффициент отражения 98 %, ванна 3: (9 и 12 мин, 15,5 А). /дм2, 333К или 343К и 353К) - коэффициент отражения = 99%. |
| j = 50 ± 2, 1000 ± 10 А/дм2, Т = 65 ± 5, 55 ± 5 °С. | 1 — H3PO4 (20 % об/об), H2SO4 (80 % об/об). 2 — H3PO4 (80 % об/об), H2SO4 (20 % об/об). | Химический состав поверхности, модуль Юнга/304L, 316L, размеры образца: 30 х 5 х 1 мм. | XPS-анализ: отношение Cr/Fe после ЭП (1000 А/дм2) = 1,5 в ванне 1, отношение Cr/Fe после ЭП (1000 А/дм2) = 2,7 в ванне 2, Ванна 1: модуль Юнга выше для ЭП (50 А/дм2) дм2), чем для ЭП (1000 А/дм2). Толщина слоя h для стали 316L, после ЭП (50 А/дм2): PO43- >> SO 4 2- h = 10 нм, PO3- > SO42- h = 3 нм, PO43- h = 12 нм, после ЭП (1000 А/дм2): PO43- SO42- h = 7 нм, PO43- > SO42- h = 3 нм, PO43- h = 3 нм, Ванна 2: модуль Юнга выше после ЭП ( 1000 А/дм2), чем после ЭП (50 А/дм2). Толщина слоя h для стали 316L, после ЭП (50 А/дм2): PO43- >> SO42- h = 10 нм, PO3- > SO42- h = 5 нм, PO43- h = 10 нм, после ЭП (1000 А/дм2): PO43-? = 3 нм,PO43- >> SO4 2- = 17 нм, PO3-= 15 нм. |
| I = 1 А, j = 12,9 А/дм2, Т = 55 ± 5 °С, S = 7,78 см2. | H3PO4, H2SO4, H2O. | Химический состав поверхности/316L, размеры образца: 19 х 19 х 0,737 мм. | Увеличение ат. % содержания Cr в верхнем слое с 16 % после механической обработки до 20 % после ЭП. Снижение ат. % содержания Fe в верхнем слое с 18 % после механической обработки до 10 % после ЭП. |
| j = 0,29 А/дм2, t = 1 ч. | H3PO4 (430 мл), H2SO4 (25 мл), CrO3 (30 г). | Химический состав поверхности/316. | AES SS: ат.% Fe = 27%, травление: ат.% Fe = 25%, шлифование: ат.% Fe = 20%, травление + EP: ат.% Fe = 16%, шлифование + EP: ат.% Fe = 30 %, нержавеющая сталь: ат. % Cr = 7 %, травление: ат. % Cr = 8 %, шлифование: ат. % Cr = 5 %, травление + EP: ат. % Cr = 3 %, шлифование + EP : ат.% Cr = 16%, SS: ат.% Ni = 4%, протравленный: ат.% Ni = 4%, отшлифованный: ат.% Ni = 3%, протравленный + EP: ат.% Ni 2% , отшлифованная + EP: ат.% Ni = 3%, отшлифованная: ат.% Si = 22%.SS: ат.% C = 4%, протравленная: ат.% C = 15%, отшлифованная: ат.% C = 25%, SS: ат.% O = 50%, травление: ат.% O = 45%, шлифование: ат.% O = 16%, травление + EP: ат.% O = 56%, шлифование + EP: при .% О = 40%. |
|
U = 40 В, t = 75 с. j = 500 А/дм2, 1000 А/дм2, T = 60 ± 1 °C. |
HClO4 (20% по объему), CH3COOH (80% по объему). H3PO4, H2SO4. |
Химический состав поверхности/316L Размеры образца: 12 х 5 х 3 мм. Химический состав поверхности/316L Размеры образца: 25 х 5 х 1 мм. |
EDS SS: ат.% Fe = 33,21 ± 0,89%, после МП (механическая обработка): ат.% Fe = 34,72 ± 3,22%, после ЭП: ат.% Fe = 31,95 ± 2,72%, SS: ат.% Cr = 1,18 ±0,03 %, после МП: ат. % Cr = 1,21 ± 0,02 %, после ЭП: ат. % Cr = 1,31 ± 0,19 %, СС: ат. % Ni = 2,32 ± 0,35 %, после МП: ат. % Ni = 2,72 ± 0,41 %, после ЭП: ат. % Ni = 4,63 ± 1,00 % SS: ат. % O = 63,12 ± 0,9 %, после МП: ат. % O = 61,35 ± 2,83 %, после ЭП: ат. % O = 62,10 ± 3,89%.XPS: отношение Cr/∑E4 (Fe, Cr, Ni, O) после ЭП (500 А/дм2): Cr/∑E4 = 0,0807, отношение Cr/SE4 (Fe, Cr, Ni, O) после МЭП (225/50 A) /дм2): Cr/∑E4 = 0,0397, отношение Cr/∑E4 (Fe, Cr, Ni, O) после МЭП (225/1000 А/дм2): Cr/∑E4 = 0,0673. |
| j = 50 ± 2 А/дм2, 1000 ± 10 А/дм2, T = 65 ± 5, 75± 5 °С | 1—H3PO4 (60 % по объему), H2SO4 (40 % по объему) 2—H3PO4 (40 % по объему), H2SO4 (60 % по объему) | Химический состав поверхности/316L Размеры образца: 30 х 5 х 1 мм. | XPS: сигнал Fe2p ниже после ЭП (1000 А/дм2) в ванне 1, чем после ЭП (50 А/дм2), мин. Содержание Fe (ат. % Fe = 2,5 %) после ЭП (1000 А/дм2) в ванне 1, ат. % Cr2p (Cr6+) после ЭП: (50 А/дм2) = 1,6 %, ат. % Cr2p (Cr6+) после ЭП: (1000 А/дм2) = 23,2%. |
| U = 10 В, T = 60 °C. | H2SO4, H3PO4 – об. 1:3. | Химический состав поверхности/316LVM. | XPS: после ЭП: ат. % Cr = 1,8 %, после МЭП (магнитно-электрохимической полировки): ат. % Cr = 10,1 %, после ЭП: ат. % Mo = 0,4 %, после МЭП: ат. % Mo = 1,9 % , после ЭП: ат. % Fe = 15,4 %, после ЭП: ат. % Fe = 9,7 %, после ЭП: ат. % S = 1,5 %, после МЭП: ат. % S = 3,9 %, после ЭП: ат. % Р = 17,2%, после МЭП: ат.% Р = 16,4%. |
| I = 2,5 А, j = 65 ± 5 А/дм2, Т = 65 ± 5 °С, t = 3 мин, S = 3,854 см2, q = 32 мАч/см2. | H3PO4, H2SO4 – об. 4:6. | Химический состав поверхности/430 SS, размеры образца: 30 х 5 х 1,22 мм. | XPS: после МП (механическая обработка) отношение Cr/Fe = 0,4, после ЭП: отношение Cr/Fe = 2,25, после ЭП (электрохимическая полировка с перемешиванием) соотношение Cr/Fe = 0,96, после МЭП (магнитно-электрохимическая полировка) Cr/Fe коэффициент = 0,7. |
| j = 50 ± 1 А/дм2, 1000 ± 10 А/дм2, Т = 65 ± 5°С, 55 ± 5 °С. | H3PO4 (20 % по объему), H2SO4 (80 % по объему). | Химический состав поверхности/дуплексной стали 2205. Размеры образцов: 30 х 5 х1 мм. | Сигнал Fe2p ниже после ЭП (1000 А/дм2), чем после ЭП (1000 А/дм2), после ЭП (50 А/дм2) отношение Cr/Fe = 1,9, после ЭП (1000 А/дм2) отношение Cr/Fe = 1,7 , после ЭП (50 А/дм2) отношение P/S = 0,5, после ЭП (1000 А/дм2) отношение P/S = 0,3. |
| U = 8 В, 9,5 В; t = 15 мин, 20 мин. | H2SO4 96%, H3PO4 85% — мас. 1:1. | Твердость/316L. | Микротвердость по Виккерсу SS: VHN = 168,27 кг/см2, после шлифования VHN = 283 кг/см2, после шлифования и EP VHN < 205 кг/см2. |
| j = 20 А/дм2, T = 55± 2 °C, t = 2–4 мин S = 20 см2, q = 7–13 мАч/см2. | H3PO4 (35% по объему), H2SO4 (60,5% по объему), триэтаноламин (4,5% по объему). | Твердость/316L Размеры образца: 80 х 20 х 2 мм. | Микротвердость по Виккерсу SS: 188 HV, после МП: 318 HV, после ЭП образцы характеризовались более низкой микротвердостью 230 HV. |
| j = 4–8 А/дм2, T = 35–55 °C, t = 15–45 мин. | H3PO4, H2SO4, триэтаноламин (3 мас.%). | Поверхностные дефекты, ванны с /304 площадью поверхности ок. в промышленных условиях 33,3 дм2, в лабораторных условиях 0,4 дм2. | Не оптимальные варианты технологических параметров (плотность тока, температура) приводили к возникновению дефектов на поверхности электрохимически полированных образцов. Плохое качество поверхности отражалось высокими показателями шероховатости, превышающими 0,24 мкм и даже достигающими 0,55 мкм, и низкими значениями блеска, ниже 500 ед. Рекомендуемые параметры: T = 35 °C, j = 8 А/дм2. |
Обозначения, применяемые в таблице:
шероховатость поверхности (с использованием АСМ или профильного измерителя), химический состав поверхности (EDX, AES и XPS), блеск поверхности, устойчивость к коррозии, химический состав ванны для электрополировки, адгезию клеток/бактерий к обрабатываемой поверхности и твердость поверхностей образцов. Эксперименты были проведены для нержавеющих сталей: 304, 316L, 316LVM, 430 и duplex 2205. Измеренные 2D и 3D
Показатели шероховатости:
- Ra (мкм, нм) — среднее арифметическое отклонение профиля поверхности от средней линии, измеренной вдоль измерительного или элементарного участка;
- Rq (мкм, нм) — среднеквадратичное отклонение профиля поверхности от средней линии, измеренной вдоль измерительного или элементарного участка;
- Rz (мкм, нм) — максимальная высота шероховатости от средней линии, измеренной вдоль измерительного или элементарного участка;
- Rp (мкм, нм) — максимальная высота пика профиля;
- Rv (мкм, нм) — глубина самого глубокого углубления профиля;
- Sa (мкм, нм) — среднее арифметическое отклонение шероховатости поверхности от плоскости отсчета;
- Srms (мкм, нм) — среднеквадратичная шероховатость поверхности.
Показатели коррозионных испытаний:
- OCP (V) — потенциал разомкнутой цепи;
- Ecor (mV, V) — коррозионный потенциал;
- Epit (V) — потенциал точечной коррозии;
- Vp (мм/год) — скорость коррозии.
Необработанные/измельченные образцы были обозначены как SS, образцы после механической полировки — как после MP, после электрохимической полировки - после EP, после магнитно-электрохимической полировки - после MEP.
В исследованиях, представленных выше, качество поверхности и эффект сглаживания поверхности обычно контролировались путем анализа профиля шероховатости Ra (нм, мкм). После электрохимической полировки удалось получить более низкие значения Ra для необработанных образцов и образцов, ранее подвергнутых механической или химической обработке. Электрополировка снизила шероховатость поверхности Ra образцов имплантатов, изготовленных из стали 316L, с 18,4 ± 4,5 нм (АСМ) и 183,1 ±80,6 нм (профильный измеритель) до 2,1 ± 0,8 нм и 76,2 ± 67,9 нм. Химическое травление и механическая обработка также уменьшили параметр шероховатости Ra, по сравнению с исходным образцом - SS: Ra = 120,52 ± 26,65 нм, после травления: Ra = 126,07 ± 37,13 нм, после осслабления: Ra = 142,71 ± 26,20 нм, после EP: Ra = 13,13 ± 1,56 нм.
В другом исследовании был получен более низкий параметр Ra образцов EP (Ra < 0,11 мкм) после предыдущего травления (Ra = 0,37–0,43 мкм) сравнение с исходными образцами (Ra = 0,17–0,25 мкм).
Химический состав образцов в основном анализировался с помощью рентгеновской фотоэлектронной спектроскопии (XPS). Поверхность образца анализировалась как в исходном состоянии, непосредственно после обработки, так и после дополнительная очистка ионами Ar+. Тестирование показало, что состав пассивного слоя после ЭП был обогащен хромом (оксиды и гидроксиды хрома), содержание которого для образца SS составляло: при.% Cr = 5,7% ат. и после ЭП: при.% Cr = 11,5% ат. Аналогичная корреляция была получена в других исследованиях, где наблюдалось увеличение ат.% Cr с 16% (механически обработанный образец) до 20% после эпоксидирования, наряду со снижением содержания Fe (оксидов железа) в верхнем слое: после механического обработка: при.% Fe = 18%, после EP: при.% Fe = 10%. Низкое соотношение содержания оксидов железа к общему содержанию оксида и гидроксида хрома может способствовать повышению коррозионной стойкости пассивных слоев, полученных в результате ЭП.
Качественный анализ химического состава поверхности также был проведен с использованием энергодисперсионной рентгеновской спектроскопии (EDS). Содержание хрома в пассивном слое увеличилось с 18,83 мас.% до 19,33 мас.% после электрохимической полировки. В ходе испытаний также был проанализирован блеск поверхности до и после EP. После первоначальной подготовки образцов (шлифовки) блеск G = 400, в то время как после EP блеск увеличился до G = 1700-2500.
Коррозионная стойкость была определена в потенциодинамических исследованиях. На основании полученных результатов было установлено, что коррозионная стойкость нержавеющей стали 304 и 316L значительно улучшилась. Высокое содержание хрома в обоих этих типах стали обеспечивает образование пассивного слоя, который защищает материал от воздействия агрессивной среды на поверхности элементов.
Измерения поляризации показали заметное улучшение стойкости к точечной коррозии и сдвиг потенциала точечной коррозии в сторону более положительных значений. Для образцов после EP значение Epit составляло 0,57 В, и оно было заметно положительнее, чем для протравленных образцов Epit = 0,38 В и необработанных образцов Epit = 0,30 В (по каломельному электроду сравнения). В других исследованиях Ecor для механически обработанной поверхности составлял -0,533 В, в то время как после EP: Ecor = -0,324 В. Аналогичная корреляция была обнаружена в исследовании. После травления Ecor составлял -0,326 В, а после электрохимической полировки Ecor = -0,173 В. Представленные результаты исследований позволяют нам утверждать, что электрополировка повышает коррозионную стойкость по сравнению с необработанными образцами, травлеными или механически обработанными.
В другом интересном исследовательском проекте анализировалась адгезия клеток крови к поверхности образцов из стали 316L-SS после электрохимической полировки при напряжении постоянного тока U = 2,5, 4 и 10 В (T = 65-70 °C, t = 3 мин). Наряду с уменьшением шероховатости поверхности SS: Ra = 188 ± 9 нм, EP (2,5 В) Ra = 107 ± 6 нм, EP (4 В) Ra = 77 ± 4 нм, EP (10 В) Ra = 97 ± 11 нм и повышением коррозионной стойкости: SS: OCP = 0,34 В, EP (2,5 В) OCP = 0,29 В, EP (4 В) OCP = 0,18 В, снижение адгезии выхода клеток крови с поверхности стали 316L наблюдался для образцов после ЭП: при 2,5 В - на 71%, при 4 В – на 89% и при 10 В - на 93%. Это исследование позволяет нам утверждать, что электрополировка значительно способствует снижению адгезии клеток крови к поверхности обрабатываемых элементов (стентов), что оказывает существенное влияние на тромбогенность.
Электрохимическая полировка также снижает адгезию бактерий к поверхности элементов из нержавеющей стали, используемых в тяжелой, пищевой, фармацевтической и медицинской промышленности. Адгезия бактерий к поверхности устройств (образование биопленки) может привести к загрязнению продукта за счет проникновения патогенных микроорганизмов из биопленки и к повреждению или разрушению поверхности из нержавеющей стали. После ЭП количество бактерий на поверхности нержавеющей стали уменьшилось на 79% и 94% соответственно. Электрохимическая обработка может оказать значительное влияние на повышение устойчивости к образованию бактериальной биопленки на поверхности устройств.
Процесс электрополировки также влияет на микротвердость обрабатываемых элементов.
Микротвердость необработанных образцов составила 168,27 кг/см2, после шлифования -283 кг/см2, в то время как после шлифования и EP < 205 кг/см2. Приведенные выше результаты указывают на то, что микротвердость материала, подвергнутого механической обработке, выше, чем после электрохимической полировки. Шлифование приводит к упрочнению при холодной обработке, что оказывает значительное влияние на результаты микротвердости. Сжатие после механической обработки может быть частично устранено электрополировкой. Образцы после механической обработки характеризовались более высокой микротвердостью, чем образцы после механической обработки, и электрохимическая полировка.
Дефекты поверхности были обнаружены после процесса электрополировки в промышленных условиях. Для испытаний использовали ванну, содержащую H3PO4 и H2SO4 и триэтаноламин, загрязненные в промышленных условиях, железом около 3% по массе.
В промышленных испытаниях были использованы образцы площадью приблизительно 33,3 дм2. Для сравнения были проведены лабораторные испытания с площадью образцов 0,4 дм2. Результаты лабораторных исследований позволяют оцените потерю веса, которая будет получена в промышленных условиях, с учетом использования того же электролита. Из-за ограничений в промышленных условиях и многократной электрополировки крупногабаритных заготовок используемый диапазон плотности тока составлял 4-8 А/дм2, диапазон температур 35-55 °C.
Самые явные эффекты были получены при низкой температуре и плотности тока 8 А/дм2. Сочетание низкой плотности тока и высокой температуры привело к неравномерной полировке образца и “эффекту апельсиновой корки". С одной стороны, поверхность отполирована, с другой - вид текстурных неровностей, похожий на кожуру апельсина (рисунок 1). Кроме того, “эффект апельсиновой корки” встречался на металлах и сплавах с грубой кристаллической структурой, поскольку оксидная, адсорбционная и диффузионная пленки, которые смещают потенциал анода далеко от термодинамического равновесия, характерного для процесса анодного травления, когда эти пленки не способны преодолеть эффект преимущественного влияния активных центров на аноде. Это тот случай, когда поверхность блестящая, но не гладкая.

Рисунок 4 - Металлографические фотографии аустенитной хромоникелевой нержавеющей стали: а - в состоянии поставки, б – глянцевая поверхность после ЭП (Т = 35 ◦С, 8 А/дм2), в – кромка образца с глянцевой поверхностью после эп, г - внутренняя область образца с эффектом апельсиновой корки после эп.
Были также представлены дефекты, такие как полосы электрополировки (образование и перемещение кислорода). После процесса электрополировки на поверхности могут появиться определенные дефекты, в том числе возникшие в результате длительного использования электролита, неправильной плотности тока или локального перегрева. Дефекты могут быть результатом неоптимальных параметров, состава партии и загрязнения. К наиболее распространенным дефектам относятся эффект апельсиновой корки, тени, подтеки, разводы и неравномерная полировка материала.
Параметры процесса электрополировки, состав ванны и загрязнения играют важную роль в возможности возникновения дефектов.
При выборе технологических параметров следует также учитывать форму и размер электрополированных образцов. Некоторые исследователи даже использовали высокие температуры 75-95°C для электрохимическая полировка небольших образцов.
При электрополировке крупногабаритных деталей и необходимости использовать минимально возможную плотность тока, часто в диапазоне 4-5 А/дм2, в зависимости от степени загрязнения электролита, также можно использовать температуру ниже 50°C. Подача большого тока может привести к пригарам. В целом электролиты, допускающие более низкие плотности тока, предпочтительнее.
Приложения

Рисунок 5 - График изменения поверхностного натяжения a электролита, массовые доли в %: H2SO4 (1,84) 50-60; H3PO4 (1,68) 50-40 в зависимости от природы и концентрации добавки ПАВ:
1- сульфопонат; 2 - мононатрий-альфасульфопальмитат; 3 - полиэтиленполиамин; 4 - карбоксиметилцеллюлоза; 5 - неонол; 6 - 0,3г/л карбоксиметилцеллюлоза+мононатрий--альфа-сульфопальмитат
Рисунок 6 - График изменения поверхностного натяжения a электролита: массовые доли в % H2SO4 - 20%, H2PO4 - 60%, H2O - 20% на границе фаз при добавке: 1 - синтанола; 2 - сульфоуреида; 3 - сульфопоната; 4 - сульфопоната с 0,01 г/л пеногасителя ПМС-200 А
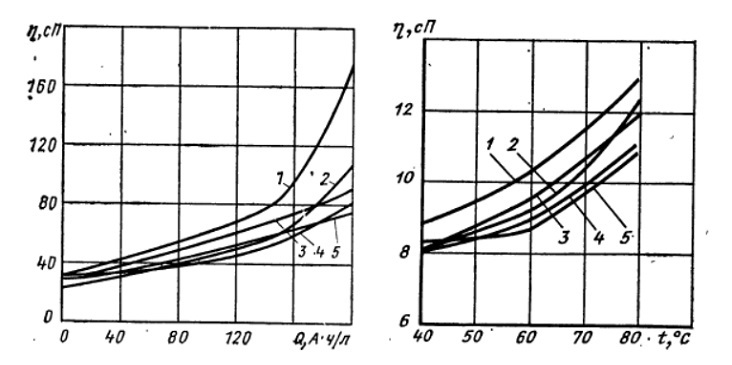
Рисунок 7 - Зависимость вязкости сернофосфорнокислого электролита для полирования стали 08Х18Н10Т от количества пропущенного электричества и природы добавки ПАВ при 60 °C:
1 - сульфоуреид; 2 - электролит без добавки; 3 - сульфопанат; 4 - полиакриламид; 5 - карбоксиметилилцеллюлоза
Рисунок 8 - Зависимость вязкости сернофосфорнокислого электролита для полирования стали 08Х18Н10Т от температуры его обработки и природы ПАВ, Q = 100А*ч/л:
1 - сульфопонат + ПМС-200 А; 2 - электролит без добавки; 3 - полиакриламид; 4 - сульфоуреид; 5 - карбоксиметилцеллюлоза
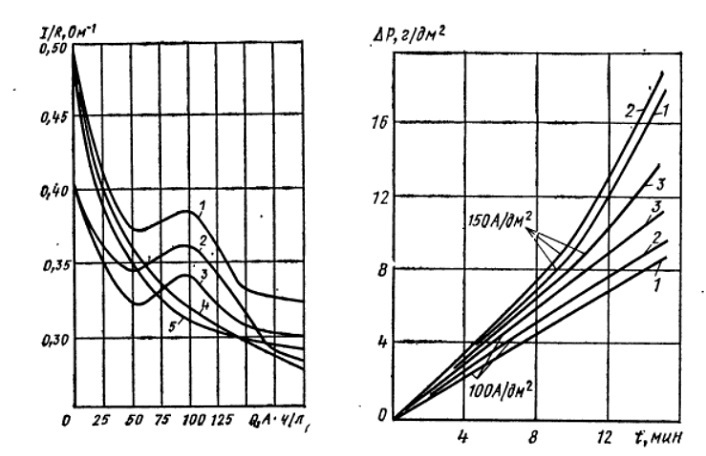
Рисунок 9 - Зависимость электропроводности сернофосфорнокислого электролита для полирования стали 08Х18Н10Т от количества пропущенного электричества и природы добавки ПАВ при 45 °C:
1 - карбоксиметилцеллюлоза; 2 - полиакриламид; 3 - чистый без добавки; 4 - сульфоуреид; 5 - сульфопонат+ПМС-200А
Рисунок 10 - График Изменения скорости съема стали при электрохимическом полировании стали 12х18н9т в сернофосфорном (1) сернофосфорнохромовом (2) и сернофосфорном электролите с добавкой ПАВ и пеногасителя (3) при различной плотности тока
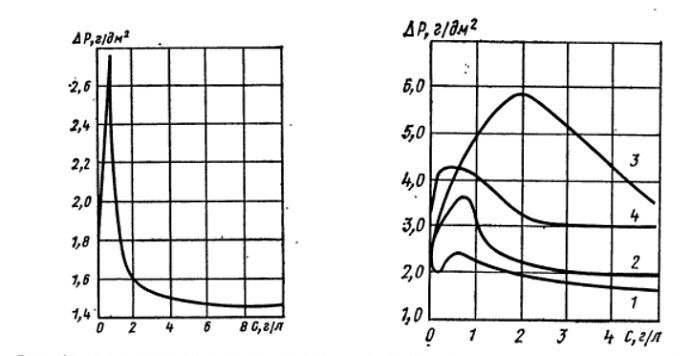
Рисунок 11 - Зависимость съема стали 12Х18Н10Т от концентрации ПАВ (сульфопонат) в сернофосфорном электролите ( i = 200А/дм2; T = 60 °C; t = 3 мин)
Рисунок 12 - Зависимость съема стали 08кп от концентрации добавок в электролите (H2SO4: H3PO4 = 50:50):
1 - карбоксиметилцеллюлоза; 2 - этансульфонат целлюлоза; 3 - сульфопонат; 4 - ОП-10
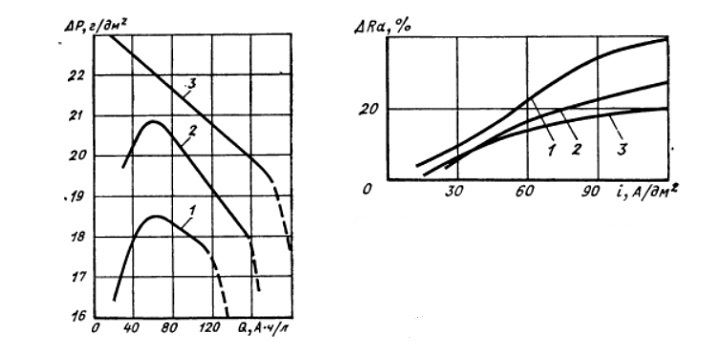
Рисунок 13 - Изменения съема металла в зависимости от количества пропущенного электричества:
1 - сернофосфорнохромовый электролит (7% CrO3); 2 - сернофосфорный; 3 - сернофосфорный с сульфопонатом (2г/л) и пеногасителем А-154 (0,5 г/л)
Рисунок 14 - График влияния соотношения фосфорной и серной кислот в электролите на относительное сглаживание стали 30х13Л при различных соотношениях (в %) H3PO4 : H2SO4:
1- 80:20, 2 - 60:40, 3 - 50:50
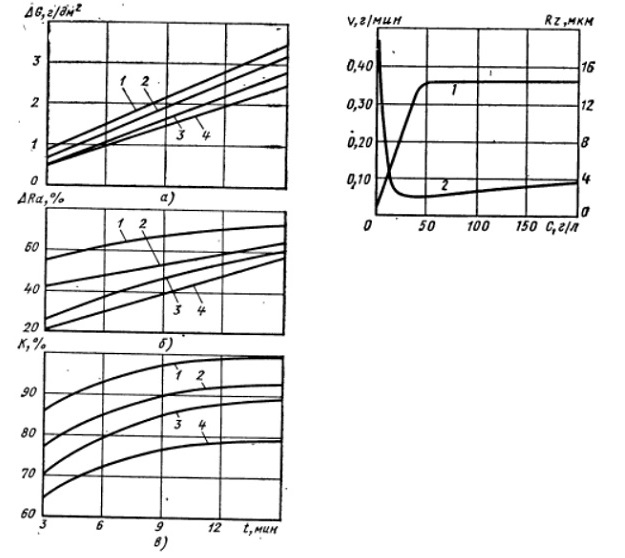
Рисунок 15 - График влияния длительности обработки на съем металла G (a), относительное сглаживание ΔR а (б) и отражательную способность K (в) сталей:
1 - 55; 2 -55г; 3 - 55г2; температура 20 °C; плотность тока 60А/дм2; электролит (объемные доли в %); H3PO4 90, H2SO4 10 + 2г/л ПАВ (РМК)
Рисунок 16 - График влияния добавки едкого натра к электролиту (100г/л NaNO3) на скорость растворения (1) и высоту микронеровностей (2) при электрохимическом полировании вольфрама

Рисунок 17 - Зависимость блеска поверхности от частоты ƒ прямоугольного тока при полировании титана в 10% - ном формамидном растворе суотфаминовой кислоты. Анодная плотность ia = 20А/дм2; катодная плотность ik - 5 А/дм2; ta = tk, общая длительность 20 мин
Рисунок 18 - Зависимость блеска поверхности от анодной плотности тока при полировании титана в 10%-ном формамидном растворе сульфаминовой кислоты:
J - постоянный ток; 2 - прямоугольный ток частотой перемен 40 Гц при ik = 5А/дм2, ta = tk; 3 - то же, с добавкой HCL

Хотите стать нашим клиентом?
Просто оставьте Вашу заявку, заполнив форму справа и мы свяжемся с Вами в ближайшее время. Спасибо!

Отправляя заявку, Вы даете согласие на обработку Ваших персональных данных. Ваши данные под защитой.



