
Теоретические основы кристаллизации металлов из растворов под действием электрического тока.
1. Общие сведения об электрокристаллизации металлов.
Механизм электрохимических процессов, в частности электродных, достаточно сложно объяснить не вдаваясь в теорию электрокристаллизации металлов. Сбор установки для ведения электродных процессов не является чем-то сложным или требующим особой квалификации, но исследование электродных процессов является серьезной задачей.
Основные причины, осложняющие исследование – это многостадийность катодных и анодных процессов, а также наличие молекул воды, которые по своей природе являются дипольными, т.е. центры их «+» и «-» зарядов находятся в разных местах. При воспроизведении электродных процессов, находящиеся в растворе катионы металлов буду окружены оболочкой из дипольных молекул воды, так как катионы являясь положительно заряженными. Они притягивают к себе отрицательный полюс молекулы воды и отталкивают положительный.
Электрохимический процесс поучения металлических покрытий представлен двумя группами реакций.
• На катоде происходит восстановление ионов металла:
Mn+ + ne- → M
Этот процесс чаще всего носит стадийный характер.
В свою очередь на растворимом аноде происходит противоположный процесс окисления, т.е. растворение металла из которого анод состоит:
Mn+ - ne- → M
Если же анод нерастворимый, то на нем будут идти другие реакции окисления, в основном - выделение кислорода.
2. Кинетика катодных процессов кристаллизации металлов из водных растворов.
Рассмотрим стадийную структуру катодного процесса:
- I стадия — движение сольватированных катионов к катоду. На поверхности катода происходит частичное разрушение водной оболочки и адсорбция.
- II стадия — переход электронов от катода к электронной оболочке катиона, что приводит к превращению катионов в нейтральные атомы металла. В момент возникновения нейтральные атомы адсорбируются на катоде.
- III стадия — катодный процесс продолжается в двух направлениях – образовавшиеся нейтральные атомы либо создают на поверхности новые кристаллы (зародыши) либо помогают росту уже образованных зародышей.
Скорость электрохимической реакции определяется т.н. называемой лимитирующей стадией – стадией с наименьшей скоростью протекания. При этом, замедление какой-либо из стадий приводит к перенапряжению на катоде и сдвигу значения потенциала катода в отрицательную область. Данное явление называется поляризацией и характеризуется следующим уравнением:
ή = Ep - Ei
где:
Ei — потенциал электрода под током, В;
Ep — равновесный потенциал, В.
Научно доказано, что с увеличением значения электродной поляризации уменьшается величина образуемого зерна металла. Поэтому используются все возможности создания благоприятных условий для увеличения поляризации.
Благодаря разнообразию электродных процессов существует множество различных перенапряжений: переходное, диффузионное, реакционное, кристаллизационное и др.
Диффузионное перенапряжение ήd возникает в результате снижения концентрации компонентов в ДЭС (двойном электрическом слое), что в свою очередь является следствием низкой скорости диффузии компонентов из объема электролита к поверхности катода. Для вычисления значения диффузионной поляризации используется уравнение Нернста.
ήd = (RT/nF) ln(c1/c0)
где:
c1 — концентрация потенциалоопределяющих ионов в прикатодном слое;
c0 — концентрация тех же ионов вдали от электрода;
n — их валентность;
R — газовая постоянная;
Т — абсолютная температура;
F — число Фарадея.
Учитывая, что:
c1 = c0 (1 - (i/id))
где:
i — плотность тока, поляризующего электрод;
id = Kc0 — плотность предельного тока диффузии исходных веществ к электроду;
К — константа,
в конечном итоге получаем уравнение:
ήd = (RT/nF) ln(1 - (1/id))
Из данного равенства следует, что факторы, ускоряющие доставку реагентов к катоду, увеличивают поляризацию. Такими факторами являются перемешивание, повышение температуры и т.д.
Реакицонное или химическое перенапряжение ήr появляется в следствии замедления отдельных стадий реакции на катоде. Связь химического и диффузионного перенапряжений позволяет объединить их в т.н. концентрационное перенапряжение ήc , что соответствует уравнению:
ήc = hd + hr
Торможение электродной реакции может быть вызвано переносом электронов через ДЭС. В процессе разрушения водной оболочки катионов и освобождения их от лигандов возникает переходное напряжение ήп в свою очередь, определяется уравнением Тафеля:
ήп = a + b log i
где:
i — плотность тока, А/дм2;
а и b — константы, определяемые опытным путем.
Кристализационное перенапряжение ήк является следствием адсорбции ионов на катоде и их последующего встраивания в кристаллическую решетку. Кристаллизационное перенапряжение зависит в основном от тока обмена i0.
Легко проследить связь кристаллизационного перенапряжения, тока обмена и величины образуемого зерна можно при использовании простых солей для осаждения металлов. В данном случае другие виды перенапряжения не являются сколь-нибудь значимыми.
В зависимости от величины ήк можно разделить все металлы на 3 основные группы:
- Металлы, имеющие высокие значения тока обмена 101 - 10-2 А/см2. В процессе их осаждения, значение перенапряжения находится в пределах нескольких милливольт. К данной группе относятся серебро, кадмий, олово. Данные металлы образуют крупнокристаллические покрытия с размером зерна в пределах десятка мкм;
- Металлы, значения токов обмена которых находятся в средней области 10-4 - 10-5 А/см2, образуются покрытия с размером зерна от 1 до 10 мкм. К данной группе относятся висмут, медь, цинк;
- Последняя группа – металлы, образующие мелкокристаллические покрытия с величиной зерна от 0,01 до 0,001 мкм. Металлы данной группы имеют самые низкие токи обмена 10-8 - 10-9 А/см2. К данной группе относятся кобальт, железо, никель.
Химическое, переходное и кристаллизационное перенапряжение в сумме дают общее перенапряжение ή процесса, которое выражается уравнением:
ή = ήc + ήп + ήк
Отсюда можно сделать вывод, что образование кристаллов на катоде происходит при изменении потенциала катода в отрицательную область.
Чем меньше размер кристаллов покрытия, тем плотнее его структура и лучше эксплуатационные свойства.
3. Основы электрокристаллизации металлов.
3.1 Кинетические закономерности.
Хотя изучение процесса электрокристаллизации является достаточно сложной темой, механизм процесса соответствует законам, аналогичным законам образования кристаллической фазы при использовании расплава или раствора (например, замерзание воды или выкристализовывание солей).
Кинетические закономерности процесса электрохимической кристаллизации зависят от двух параметров:
- Скорости образования зародышей (центров кристаллизации);
- Скорости роста зародышей.
Размер отдельных образующихся кристаллов зависит от соотношения скорости образования новых и роста старых.
- Если скорость образования новых кристаллов выше скорость их роста, происходит образование мелкокристаллической структуры.
- В противоположном случае, получается крупнокристаллическая структура.
Основной фактор, оказывающий влияние на скорость образования зародыша – степень пересыщения раствора. Данный фактор характеризуется уравнением:
b = с/cн
где:
с — концентрация кристаллизационного раствора;
cн — равновесная концентрация насыщенного раствора.
Чем больше отклонение значения b от 1, тем выше скорость зародышеобразования. В случае с расплавами, степень пересыщения заменяется на степень переохлаждения жидкости. В рассматриваемом процессе электрокристаллизации металла, вместо степени пересыщения принята величина, прямо пропорциональная плотности тока:
b = i/i0
где:
i — плотность тока процесса;
i0 — ток обмена.
Поправку вносит тот факт, что значение тока обмена зависит от природы используемого металла. Таким образом, при одном и том же значении плотности тока, при использовании различных металлов образуются различные по структуре покрытия. Общим, как указывалось выше, является тот факт, что при увеличении плотности тока для любого металла происходит уменьшение размеров зерен.
Для образования кристалла необходимо образование зародыша критического размера. Благодаря тому, что катодная поверхность на границе с раствором находится в не активном состоянии, необходимо начальное перенапряжение для образования первых зародышей. В дальнейшем, для роста зародышей не требуется дополнительная поляризация, поэтому перенапряжение уменьшается до достижения равновесного состояния.
Любое кристаллическое тело имеет в своем составе множество кристаллов, называемых кристаллитами или зернами. Размер отдельных зерен варьируется в пределах от 0,1 до 10 мкм.
Существует 3 вида зародышей:
- Одномерный зародыш — цепочка атомов;
- Двумерный зародыш — «полянка» атомов;
- Трехмерный зародыш — кристалл.
Для образования новых зародышей, предпочтительны двумерные и трехмерные зародыши.
На рисунке 1 представлена схема роста двумерных зародышей.
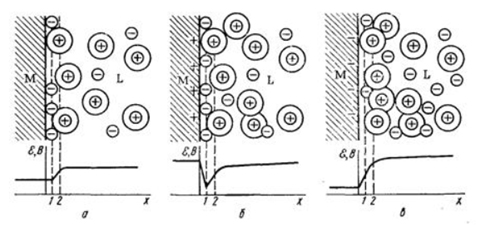
Рисунок 1 — Схема роста зародышей.
Цифрами и темным цветом на рисунке обозначены места, где существует наибольшая вероятность роста кристалла. При этом, участок «1» является наиболее предпочтительным, так как атом одновременно «зацепляется» с соседними к «1» кристаллами.
Рост кристаллов будет происходить ступенчато, ряд за рядом. Когда заканчивается построение новой плоскости, начинается рост новой. Новая плоскость начинает рост как правило с середины предыдущей плоскость - кристалл «4» на рисунке 1. Периодически новая плоскость возникает до окончания строительства предыдущей, тогда рост кристаллов называют нерегулярным.
3.2 Понятие дислокации.
Данное описание роста кристаллов очень сильно упрощено. Эта схема применима только в начальный момент формирования кристалла. По мере разрастания кристаллов происходит нарушение их структуры и образование дефектов, называемых дислокациями. Дислокация - это смещение отдельных кристаллов относительно кристаллической структуры.
Скорость роста слоя кристаллов и его толщина зависит от концентрации ионов, наличия ПАВ, режима осаждения и других факторов.
При образовании нескольких дислокаций происходит их взаимодействие с образованием обрывов, спиралей, различных винтовых и краевых дефектов. На рисунке 2 представлено образование винтовой дислокации из прямолинейной ступени.
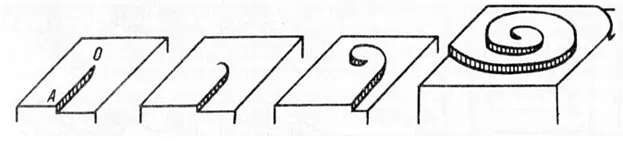
Рисунок 2 — Стадии образования винтового дефекта.
При образовании дислокаций происходит адсорбция ионов, молекул, ПАВ, что негативно влияет на оптические и электропроводные свойства получаемого покрытия.
3.3 Понятие кристаллические текстуры.
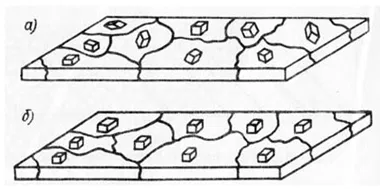
Текстура - ориентация образуемых кристаллов в различных направлениях. От текстуры зависят физико-механические свойства получаемого покрытия. В процессе образования структуры направление кристаллитов изменяется на направление параллельное оси текстуры. На рисунке 3 представлено отличие текстурированного и нетекстурированного покрытия.

Рисунок 3 — Ориентированная (а) и неориентированная (б) структура покрытия.
Серьезное влияние на текстуру будущего покрытия оказывает исходная текстура поверхности. При осаждении никеля возникает явление, называемое эпитаксией — рост кристаллов покрытия происходит по аналогии со структурой основного металла. Эпитаксиальный рост со временем может сменяться на неэпитаксиальный.
Для устранения влияния исходной структуры, возможно применение переменного тока, дополнительные промывки и перерывы в процессе нанесения покрытия. При использовании высокой плотности тока, возникает беспорядочная ориентация кристаллов. При нанесении цинкового покрытия на предварительно полированную латунную пластинку образуется мелкокристаллический осадок с беспорядочно расположенными кристалликами, а затем часть кристаллов цинка, имеющих общую ось ориентации, вырастает до значительной величины (рисунок 4).
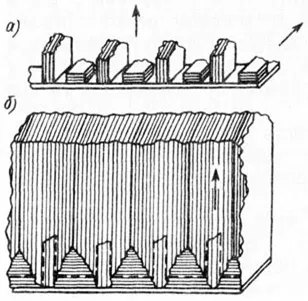
Рисунок 4 — Рост кристаллов цинка. а — начальная стадия (беспорядочная ориентация); б — конечная стадия (упорядоченная структура).
Проследить влияние отдельных параметров процесса на текстуру покрытия достаточно сложно, однако каждый из параметров может серьезно изменить физико-механические свойства покрытия.
Например, различие текстуры ферромагнетиков приводит к резкому увеличению их электропроводности и коэрцитивной силы (напряженность магнитного поля, необходимая для размагничивания ферромагнетиков), а также усилению блеска покрытия.
Учитывая многообразие требований, предъявляемых к свойствам конечного покрытия, полученного электрохимическим осаждением, нельзя преуменьшать значение получаемой текстуры.
Читайте также статьи
Что такое гальваника?
Теоретические основы нанесения гальванических и химических покрытий.
Техпроцесс нанесения белой бронзы
Что такое белая бронза? Механизм лужения. Основные электролиты и режимы процесса.
Система контроля качества
Контроляь качества гальванопокрытий на ООО

Хотите стать нашим клиентом?
Просто оставьте Вашу заявку, заполнив форму справа и мы свяжемся с Вами в ближайшее время. Спасибо!

Отправляя заявку, Вы даете согласие на обработку Ваших персональных данных. Ваши данные под защитой.



