

Хромирование | Механизм и технология гальванического процесса | Виды, структура и свойства хрома.
Содержание:
2. Механизм гальванического хромирования.
3. Основные электролиты и режимы хромирования.
4. Структура и состав хромовых покрытий.
5. Катодно-механическое хромирование (гальвано-хонингование).
1. Что такое хром?
Хром — серебристо-белый металл с синеватым оттенком. Он обладает высокой твердостью и хорошо сопротивляется механическому износу.
Хром принадлежит к числу электроотрицательных металлов, его стандартный электродный потенциал E0 (Cr0/Cr3+) равен -0,74В. В атмосферных условиях хром сохраняет цвет и блеск длительное время, что объясняется образованием на его поверхности тонкой, но очень прочной оксидной пленки. Высокой склонностью к пассивации и наличием этой пленки объясняется значительная коррозионная стойкость хромовых покрытий. В окислительных средах хром пассивируется легче, чем на воздухе и его потенциал сдвигается от стандартного в анодную область до +0,2В. Стационарный электродный потенциал хрома положительнее, чем у железа. Поэтому хромовые покрытия по отношению к стальным изделиям являются катодом.
Хром устойчив во влажной атмосфере, в атмосфере сероводорода и сернистого газа, в растворах серной, азотной, фосфорной и органических кислот, щелочей. В растворах соляной кислоты и горячей концентрированной серной хром растворяется из-за разрушения оксидной пленки.
Хромирование — процесс нанесения на поверхность изделия тонкого слоя металлического хрома для придания требуемых характеристик. Если говорить о гальваническом хромировании, осаждение металла происходит из электролита под действием электрического тока.
Хромовые покрытия широко применяются для придания изделию исключительной износо- и жаростойкости, а также для уменьшения коэффициента трения. Часто используются для придания высокодекоративного внешнего вида.
|
Обозначение |
Х - защитно-декоративное хромирование Х. тв - твердое хромирование Х. мол - молочное хромирование Х. м - матовое хромирование Х. ч - хромирование черное Chromium coating - анл. обозначение |
|
Толщина (оптимальная, возможно осадить больше) |
3-6мкм - для декоративного хромирования 15-100мкм - для твердого хромирования 24-100мкм - для молочного хромирования 15-100мкм - для матового хромирования 1мкм (не нормируется) - для черного хромирования |
|
Микротвердость |
7500 МПа - декоративное 11000 МПа - твердое 5400-6000 МПа - молочное 3500 МПа - матовое 2940-3430 МПа - черное |
|
Удельное электрическое сопротивление при 18°C |
0,15*10-3 мкОм*см |
|
Допустимая рабочая температура |
1100°C |
|
Температура плавления |
1850-1900°С. |
В соединениях хром чаще всего трехвалентен и шестивалентен. Соединения шестивалентного хрома являются сильными окислителями. Хромовый ангидрид при растворении в воде образует смесь хромовых кислот H2CrO4 и H2Cr2O7. Именно из них чаще всего и производят хромирование деталей.
В растворе хромовой кислоты имеются анионы CrO42-, HCrO4-, Cr2O72-:
- при рН > 7–8 преобладают CrO42-;
- при рН < 2-3 – Cr2O72-.
Электрохимический эквивалент хрома в хромовой кислоте составляет 0,323 г/А*ч. Но, так как выход по току металла в таких электролитах часто не превышает 10-12 %, то фактически за 1 А*ч выделяется 0,032-0,038 г хрома, т.е. в 30 раз меньше, чем никеля, в 37 раз меньше, чем меди, в 125 раз меньше, чем серебра. Единственной возможностью некоторой компенсации этого недостатка является повышение плотности тока.
В растворах трехвалентного хрома электрохимический эквивалент хрома вдвое больше, выход по току - в 4-5 раз больше, чем в хромовой кислоте.
Многочисленные попытки использовать для промышленного применения электролиты на основе трехвалентных соединений, однако, не нашли успеха, особенно для осаждения толстых износостойких покрытий.
Далее будут рассмотрены только растворы на основе шестивалентного хрома.
Электрохимическое осаждение хрома существенно отличается от других гальванических процессов:
- В большинстве электролитов, применяемых в гальванотехнике, основным компонентом является соль осаждаемого металла. При хромировании главным компонентом является хромовая кислота.
- В хромовом электролите должны присутствовать в определенном соотношении посторонние анионы: SO42-, F- или SiF62-.
- Минимальная плотность тока, при которой начинается выделение хрома, в несколько сот раз выше, чем в других процессах электроосаждения металлов.
- Электроосаждение хрома более чувствительно к изменению температуры и плотности тока по сравнению с другими гальваническими процессами. Изменение этих параметров оказывает существенное влияние не только на количественные показатели (выход по току и др.), но и на структуру и свойства осадков хрома.
- В отличие от других процессов электроосаждения металлов выход по току при хромировании резко снижается по мере повышения температуры.
Итак, основными особенностями процесса хромирования являются высокий отрицательный потенциал восстановления дихромат-анионов, низкий выход металла по току, высокие рабочие плотности тока и очень низкая рассеивающая способность электролита.
2. Механизм гальванического хромирования.
2.1 Катодные реакции.
Механизм электроосаждения хрома очень сложен. Во время хромирования на катоде одновременно протекают процессы:
- осаждения хрома;
- выделения водорода;
- восстановления шестивалентного хрома до трехвалентного;
- образования на поверхности катода тонкой пленки, состоящей из продуктов восстановления хромовой кислоты и активного аниона.
Установлено, что электролит должен содержать определенное количество активных анионов, без которых металлический хром не выделяется вообще.
Максимальное значение выхода хрома по току достигается при строго определенном соотношении между концентрацией Н2Сr2O7 и постороннего аниона.
Схематичное изображение катодных поляризационных кривых при хромировании приведено на рисунке 1. Без добавки посторонних анионов, например, сульфатов, характер кривой плавный (1), так как на электроде во всем интервале плотностей тока выделяется водород. При введении в электролит серной кислоты форма кривой усложняется (2).
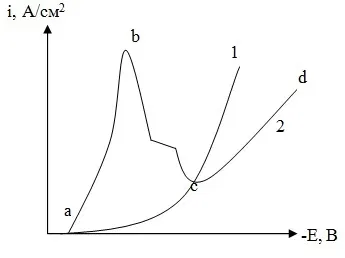
Рисунок 1 — Схематическое изображение катодных поляризационных кривых при хромировании.
Так, в присутствии сульфат-анионов кривая состоит из двух ветвей, отличающихся характером электродных реакций. При этом на участке ab происходит восстановление шестивалентного хрома до трехвалентного, на участке cd протекают одновременно три процесса — восстановление шестивалентного хрома до металла, восстановление шестивалентного хрома до трехвалентного и восстановление ионов водорода.
Анионы-активаторы изменяют поверхностное состояние катода и таким образом влияют на электродные процессы. В области кривой ab поверхность становится более активной, а в области cd наблюдается торможение реакции восстановления. Пассивность катода связана с появлением на поверхности электрода пленки из продуктов электролиза, которая лимитирует протекание одних реакций и способствует протеканию других. Обильность образования водорода объясняется низким перенапряжением его выделения на хроме.
Рассмотрим основные процессы в механизме хромирования более подробно:
а. Выделение газообразного водорода:
2H3O+ + 2e ↔ H2 + 2H2O , E0 = 0,0 B
б. Принятие электронов шестивалентным хромом с получением двух- и трехвалентных катионов с последующим осаждением металлического хрома:
Cr2O72- + 7H2O + 6e ↔ 2Cr3+ + 14OH-, E0 = +1,33 B;
Cr2O72- + 7H2O + 12e ↔ 2Cr0 + 14OH- , E0 = +0,40 B;
Cr3+ + e ↔ Cr2+ , E0 = -0,41 B;
Cr3+ + 3e ↔ Cr0 , E0 = -0,74 B;
Cr2+ + 2e ↔ Cr0 , E0 = -0,91 B.
Прежде всего должно происходить частичное восстановление шестивалентного хрома до трехвалентного состояния, совместно возможно протекание процессов восстановления ионов водорода и ионов хрома до металлического состояния. Что касается двухвалентного хрома, то наличие этих ионов в свободном состоянии в хромовой кислоте — сильном окислителе, маловероятно.
Исследователи, касающиеся вопросов восстановления шестивалентного хрома до металла, придерживаются двух основных взглядов:
- Первые допускают возможность ступенчатого восстановления шестивалентного хрома до металла.
- Вторые считают возможным непосредственное восстановление шестивалентных ионов хрома до металла.
Все исследователи согласны с тем, что на катоде при хромировании образуется особая пленка сложного состава, если покрываемая основа склонна к пассивации.
в. Синтез сложной двухслойной пленки.
Тонкий внутренний слой этой пленки аналогичен пассивным слоям (0,0001 мм), а внешний включает в себя хром в различных валентных состояниях и ионы-активаторы (до 0,025 мм). Общий состав и структура катодной пленки зависят от состава и структуры покрываемой основы. Например, на меди катодная пленка вообще не образуется, т.к. медь легко растворяется в электролите, а на железе и никеле она особенно выражена ввиду усиленной пассивации этих металлов хромовой кислотой. Катодная пленка имеет коллоидную природу, состав ее может меняться при изменении плотности тока и температуры электролита. В целом она может содержать: до 67 % шестивалентного хрома, до 23 % трехвалентного хрома, до 12% сульфат-ионов. Толщина пленки увеличивается с увеличением концентрации постороннего аниона. От свойств пленки зависит структура покрытия, а от структуры - его свойства. Именно на этом этапе формируются механические и химические отличия различных осадков хрома. Так, например, структура катодной пленки при низких плотностях тока и высокой температуре создает благоприятные условия для получения молочного хрома.
Детально механизм воздействия посторонних анионов на процесс хромирования не выяснен. Существуют две гипотезы, объясняющие их влияние:
- По первой из них анионы являются активаторами, вызывающими активацию катодной поверхности. В отсутствие этих ионов поверхность покрывается соединениями Сr3+, что препятствует полному восстановлению Н2Сr2О7 и осаждению на катоде металлического хрома.
- По второй гипотезе посторонние анионы образуют с Н2Сr2О7 реакционные комплексы, обладающие большей способностью к восстановлению последней.
На основании ряда исследований с использованием радиоактивного изотопа Cr3+ был сделан вывод, что электроосаждение хрома происходит из его шестивалентных ионов. При этом установили, что при наличии в электролите Cr3+ в виде его трехвалентных соединений осадок получался нерадиоактивным. Уже отмечалось, что из растворов coлей трехвалентного хрома качественных осадков получить не удается. Boзможно, что в электрическом поле у катода такие анионы, как Cr2O72- и Cr2O42-, деформируются, поворачиваясь своим положительным ядром к катоду. При достаточно большом потенциале Cr(VI) может быть вырван из аниона с переходом в металлическую решетку. Скорость этой электрохимической реакции определяется перенапряжением и концентрацией CrO42- у поверхности катода. Рассматривая структуру Cr2O72-, не трудно заметить, что деформация их ионов и вырывание Cr(VI) должны быть затруднены. Поэтому вполне возможно, что первым процессом, идущим при низких плотностях тока, является восстановление анионов Cr2O72- до Cr3+-ионов с одновременным подщелачиванием растворов. По достижении предельного тока для разряда Cr2O72- начинается выделение водорода, в таком случае имеет место дальнейшее подщелачивание раствора. В результате этого рН католита достигает 5-7, и тогда у катода начинают преобладать ионы CrO42-, которые, деформируясь, могут восстанавливаться как частично, так и полностью:
CrO42- + 3e + 4 H2O = Cr(OH)3 + 5OH-
CrO42- + 6e + 4 H2O = Cr0 + 8OH-
Роль SO42-, вероятно, сводится к растворению гидроокиси хрома или других коллоидных соединений, создаваемых трехвалентным хромом, т.к. они могут образовывать растворимый комплекс Cr4(SO4)4(H2O)2+. В катодном процессе ионы SO42- не участвуют, т.к. непосредственные измерения показывают, что их концентрация в прикатодном пространстве в процессе электролиза не меняется. Большое количество ионов SO42- ухудшает ocаждение, так как при этом, видимо, CrO42- могут вытесняться ими с поверхности, и выхoд по току снижается.
2.2 Анодные реакции на нерастворимых анодах.
При хромировании деталей применяют нерастворимые аноды. Это объясняется тем, что хром растворяется на аноде с бОльшим выходом по току, чем осаждается на катоде, и переходит в раствор в виде ионов разной валентности.
Анодные реакции при хромировании с участием нерастворимых свинцовых анодов следующие:
Pb + SO42- - 2e = PbSO4, E0 = +0,356 B ;
Pb + 4H2O - 4e = PbO2 + 4H+, E0 = +0,665 B ;
H2O - 2e = ½O2 + 2H+, E0 = +1,228 В ;
PbSO4 + 2H2O - 2e = PbO2 + SO42- + 4H+, E0 = +1,185 B ;
2Cr3+ - 6e + 7H2O = Cr2O72- + 14H+, E0 = +1,300 B .
В процессе электролиза аноды покрываются слоем оксида свинца (IV) РbО2, который является катализатором процесса Сr3+ → Cr6+ и защищает аноды от разрушения. При определенном соотношении анодной и катодной плотностей тока можно установить равновесие, при котором на аноде будет окисляться такое же количество трехвалентного хрома, какое попадает в электролит из катодной зоны.
3. Основные электролиты и режимы хромирования деталей.
В зависимости от режима электролиза и состава электролита могут быть получены осадки хрома с различными свойствами. В зависимости от условий электролиза образуются три типа хромовых покрытий:
- Серые осадки (обладают низкими физико-химическими свойствами и не находят практического применения);
- Блестящие осадки (отличаются высокими значениями твердости и износостойкости);
- Молочные осадки (наименее пористые и наиболее пластичные).
Кроме этого, из специальных типов электролита можно получать черные покрытия.
3.1 Универсальный раствор для хромирования.
Как правило, на практике применяют «универсальные» сульфатные электролиты хромирования. К ним относят: разбавленный, стандартный и концентрированный электролиты. Все перечисленные электролиты хромирования содержат хромовые кислоты Н2СrО4 и Н2Сr2О7 соответственно и анионы SO42- в виде серной кислоты, а также соединения трехвалентного хрома. Характеристика электролитов приведена в таблице 1.
|
Тип электролита |
Концентрация, г/л |
Характеристика |
|
|
CrO3 |
H2SO4 |
||
|
Разбавленный |
150-175 |
1,5-1,75 |
Выход по току 16-18 %. Рассеивающая способность наиболее высока. Твердость осадков самая высокая. Состав электролита в процессе работы меняется быстро, в том числе соотношение компонентов. Склонность к образованию шероховатых осадков при осаждении толстых слоев. |
|
Стандартный |
220-250 |
2,2-2,5 |
Выход по току 12-14%. Рассеивающая способность средняя. Рабочий интервал получения блестящих осадков широкий. Состав электролита меняется медленно, колебания в соотношении компонентов незначительны. Твердость осадков высокая. |
|
Концентрированный |
275-300 |
2,75-3,0 |
Выход по току 8-10%. Рассеивающая способность низкая. Электролит стабилен. Рабочий интервал получения блестящих осадков широкий. Твердость осадков самая низкая. |
В таблице 2 приведены данные по электропроводности электролитов хромирования в зависимости от концентрации хромового ангидрида при различных температурах.
|
Концентрация CrO3, г/л |
100 |
200 |
300 |
400 |
|
Удельная электропроводность, См/м при температуре 25° C |
31,5 |
51,3 |
61,6 |
66,7 |
|
Удельная электропроводность, См/м при температуре 45° C |
38,9 |
63,2 |
76,3 |
81,8 |
Разбавленный электролит позволяет получать осадки хрома высокой твердости с относительно высокими величинами выхода по току, но при этом из него получают шероховатые осадки при осаждении толстых слоев (от 100-150 мкм и более). Кроме того, омические потери напряжения в разбавленном электролите самые высокие (электропроводность низка и находится в пределах 50 См/м), что напрямую сказывается на удельных затратах электроэнергии при хромировании.
Стандартный электролит хромирования применяется на практике наиболее часто. При средних величинах выхода по току, токовых режимах хромирования 3000-6000 А/м2 и температурах 45-70° C из этого электролита осаждают толстые осадки до 300 мкм при меньших затратах электроэнергии за счет более высокой электропроводности (таблица 2), чем из разбавленного электролита. Кроме того, при температурах 45-55 °C твердость у покрытий, получаемых из разбавленных электролитов, не отличается от твердости хромовых покрытий, полученных из стандартных электролитов.
Концентрированные электролиты применяются достаточно редко, так как характеризуются низкими выходами по току при осаждении хрома и низкими твердостями осадков (практически не пригодны для износостойкого хромирования).
Следует отметить, что во всех электролитах хромирования с повышением температуры снижается величина выхода по току и увеличивается наводороживание стальной подложки. Наводороживание происходит из-за того, что одновременно с выделением хрома на покрываемой детали происходит выделение водорода, причем на этот процесс тратится большая часть тока. Наводороживание стальной основы отрицательно влияет на ее физико-механические свойства. Наиболее активно водород внедряется в металл в начальный период, когда еще не образовался сплошной слой хрома. При повышении температуры от 55° до 75° C масса поглощенного водорода увеличивается в 6-10 раз.
Величина выхода по току во всех электролитах хромирования уменьшается с повышением концентрации хромового ангидрида. Но повышенные концентрации хромового ангидрида позволяют работать при более высоких плотностях тока и за счет повышения плотности тока интенсифицировать процесс хромирования и увеличить величину выхода по току.
3.2 Тетрахроматный электролит хромирования.
Этот электролит отличается от универсальных тем, что хромовая кислота нейтрализуется щелочью и находится в виде тетрахромата натрия. Электролит рекомендуется применять в случаях:
- нанесения защитно-декоративных покрытий без подслоя меди и никеля. Толщина хромового покрытия при этом должна находиться в пределах 10-15 мкм;
- восстановления деталей хромированием, когда не требуется высокой твердости и блестящей поверхности;
- хромирования деталей со сравнительно сложной конфигурацией.
Возможность непосредственно наносить хром из тетрахроматных электролитов на сталь, латунь и цинковые сплавы объясняется тем, что в результате нейтрализации хромовой кислоты агрессивность раствора заметно снижается. В электролите образуется тетрахромат натрия по реакции:
2 NaOH + 4CrO3 = [Na2CrO(CrO4)3] + H2O
Для нормального протекания процесса необходимо поддерживать определенное соотношение между концентрацией Сr6+ и Cr3+. Это соотношение регулируется количеством вводимого восстановителя.
Вследствие высокой плотности тока электролит сильно нагревается. Во избежание разложения тетрахромата, который при температуре, превышающей 24о С, неустойчив, электролит следует охлаждать.
Выход по току в этом электролите составляет примерно 30%. При низких плотностях тока 10-25 А/дм2 осадки мягкие, матовые, cерые, с небольшими внутренними перенапряжениями. С ростом плотности тока выход по току заметно возрастает, с повышением температуры выход по току падает.
3.3 Саморегулирующийся электролит хромирования.
Хромирование в электролитах с добавками серной кислоты имеет ряд недостатков. Выход металла по току низкий. Обычно он колеблется в пределах 10-12%, состав электролита, в частности отношение CrO3 / H2SO4, в процессе работы изменяется. Последний недостаток устранен в саморегулирующихся электролитах для хромирования.
Принцип саморегулирования основан на том, что у вводимых в электролит солей сернокислого стронция и кремнефторида калия ограниченная растворимость.
Эти соли, находясь в электролите в количестве, превышающем их растворимость, при изменении концентрации ионов SO42- и SiF62- в растворе автоматически восстанавливается их соотношение.
Саморегулирующиеся электролиты менее чувствительны к изменению температуры, чем обычные сернокислые электролиты. Кроме того, они сравнительно малочувствительны к загрязнению раствора железом, медью и другими металлами. Ограничивает распространение этих электролитов то, что саморегулирующиеся электролиты оказывают растравливающее действие на некоторые металлы, в том числе и железо.
Наряду с перечисленными электролитами для холодного хромирования используется сульфатно-фторидный электролит.
4. Структура и состав хромовых покрытий.
Изменяя режим электролиза, можно получить разные типы осадков хрома, различающиеся по своим свойствам и, следовательно, областью применения. Наибольший технико-экономический эффект достигается при применении износостойкого и коррозионно-стойкого хромирования. Важно отметить, что твердость не всегда коррелирует с износостойкостью.
Диаграммы на рисунке 2 наглядно демонстрируют области получения твердых и износостойких покрытий при стандартных режимах хромирования в «универсальных» сульфатных электролитах.
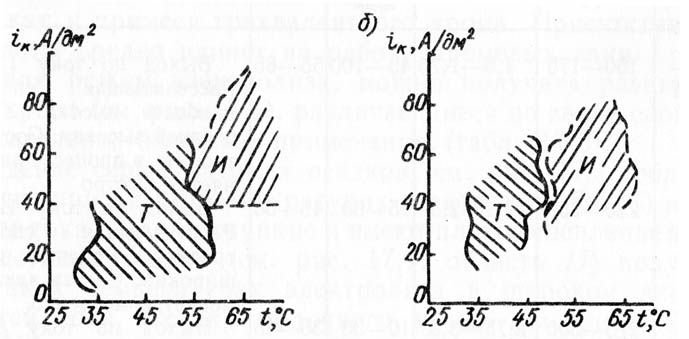
Рисунок 2 — Диаграммы условий получения твердых (Т) и износостойких (И) покрытий хромом при стандартных режимах хромирования в «универсальных» сульфатных электролитах: в разбавленном электролите (а) и стандартном электролите (б).
Износостойкость покрытий, полученных из «универсального» стандартного электролита, возрастает при повышении температуры и, пройдя через максимум при 55-65° C, снижается до минимума при 75° C. Для осадков, получаемых из разбавленного электролита, максимум износостойкости смещается в область более высоких температур. Пластичность электролитического хрома также существенно зависит от режима хромирования. Хрупкие осадки хрома (блестящие и матовые) получаются при низких температурах электролита и высоких плотностях тока, более пластичные покрытия - при высоких температурах и низких плотностях тока (молочные осадки).
Осадки электролитического хрома обладают чрезвычайно мелкой кристаллической структурой (рисунок 3).

.webp)


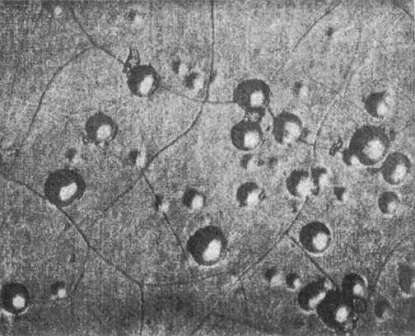

Рисунок 3 — Микроизображение (слева направо) твердого, тонкого блестящего и молочного безтрещинного хрома, х100.
Наименьшие размеры (0,001-0,01 мкм) имеют кристаллы блестящего хрома. Размеры кристаллов матового и молочного хрома 0,1-10 мкм.
Ниже приведены снимки микрошлифов поперечного среза слоя хрома при 1000-кратном увеличении (рисунок 4).


а б
Рисунок 4 — Микрофотографии поперечных шлифов матового (а) и блестящего хрома (б).
Электролитически осажденный хром содержит кислород, водород и незначительное количество азота. Массовая доля кислорода составляет 0,2-0,5 массовых долей, водорода - 0,03-0,07 массовых долей. Объем газов, включенных в осадок, зависит от температуры и плотности тока: при увеличении температуры и уменьшении плотности тока объем газов в осадке несколько уменьшается.
Известны две основные структурные модификации электролитически осажденного хрома:
- α-Cr с кубической объемно-центрированной кристаллической решеткой и плотностью 7,1 г/см3
- β-Cr с плотноупакованной гексагональной кристаллической решеткой и плотностью 6,08 г/см3.
- При высоких плотностях тока и повышенной температуре электролита образуется преимущественно кубическая структура α-Cr, при низких плотностях тока и комнатной температуре - в основном гексагональная структура β-Cr. Эта структура устойчива только при температурах ниже 25° C, а при более высоких температурах она переходит в стабильную модификацию α-Cr.
Осадкам хрома свойственны высокие внутренние напряжения, причина возникновения которых заключается в самопроизвольном переходе нестабильного β-Cr в стабильную модификацию α-Cr, имеющую более высокую плотность, в результате чего в хромовых осадках образуется сетка микротрещин. При повышении температуры электролита внутренние напряжения и число трещин уменьшаются.
Все хромовые покрытия отличаются высокой твердостью, но твердость кубического хрома значительно выше твердости гексагонального. Твердость определяется режимом электролиза, как уже упоминалось выше.
5. Катодно-механическое хромирование (гальвано-хонингование).
Анализ современных литературных источников, освещающих вопросы интенсификации процессов хромирования, а также современных российских технологий хромирования показал, что наносить блестящие хромовые покрытия на цилиндрические детали или детали типа «шток» из стандартного сульфатного электролита при плотностях тока 3000-6000 А/м2 и температурах электролита 45-70 °C позволяет технология катодно-механического хромирования (КМХ) или гальвано-хонингования. Данная технология разработана специалистами ФГУП «ЦНИИМ» (г. Санкт-Петербург).
Технология КМХ предполагает хромирование цилиндрических деталей с одновременным механическим (абразивным) воздействием на катодную поверхность, то есть совмещение процесса хромирования с хонингованием или притиркой поверхности специальными полирующими элементами. По оценкам разработчиков износостойкость хромовых покрытий, полученных с применением технологии КМХ, по сравнению с покрытиями, полученными стандартным хромированием цилиндрических деталей, возрастает в 2-4 раза [4]. Кроме того, применение катодно-механического хромирования позволяет получать толстослойные хромовые покрытия (толщиной свыше 100 мкм) с шероховатостью, соответствующей высоким классам чистоты обработки поверхности (не ниже 9 класса) без промежуточной механической обработки.
Суть процесса гальвано-хонингования - постоянная принудительная корректировка формирования поверхности в процессе хромирования полирующими элементами. Это позволяет предотвратить укрупнение неровностей с ростом толщины осадка на формируемой поверхности, предотвратить неравномерность распределения покрытия по толщине, сохранить мелкокристаллическую структуру осадка хрома (сохранение условий плоского фронта роста осадка). Другими словами, при технологии КМХ производят принудительное «выглаживание» формирующегося и растущего слоя осадка хрома на микроскопическом уровне.

Выводы специалистов-разработчиков КМХ из анализа существующих в России основных технологий хромирования цилиндрических длинномерных деталей типа «шток» свидетельствуют о следующем:
- При стандартном хромировании цилиндрических деталей для достижения необходимого класса чистоты обработки поверхности требуется механическая доводка поверхности по хрому (на дорогостоящем оборудовании), которая, как правило, снижает эксплуатационные характеристики хромового покрытия (пригары, задиры, трещины);
- При КМХ формируется покрытие с шероховатостью, соответствующей классу чистоты обработки поверхности на 2-3 единицы выше исходной чистоты обработки подложки. При этой технологии не требуется дальнейшей механической обработки хромовых покрытий, предотвращается дендритообразование, соответственно сохраняются высокие функциональные свойства хрома.
Технологические параметры и состав электролита стандартной технологии хромирования деталей не противоречат принципам технологии КМХ. Следует отметить, что гальвано-хонингование не является одновременным совмещением процесса хромирования и шлифовки поверхности, так как притирочные блоки постоянно перемещают по катодной поверхности, периодически выравнивая и полируя катодную поверхность, не истирая часть слоя хрома как при шлифовке.
Читайте также статьи
Заказать гальваническое хромирование
Сделать заказ покрытия с сертификатом качества на заводе
Все способы хромирования
Отличие методов нанесения и свойств покрытия
Влияние хрома на организм
Воздействие хрома на организм человека. Польза и вред.

Хотите стать нашим клиентом?
Просто оставьте Вашу заявку, заполнив форму справа и мы свяжемся с Вами в ближайшее время. Спасибо!

Отправляя заявку, Вы даете согласие на обработку Ваших персональных данных. Ваши данные под защитой.



